
Подписаться
Подписаться
Пути восстановления углекислого газа
 В прошлом номере мы по составу неорганических ионов в живых клетках проследили их происхождение из вод геотермальных источников и грязевых котлов. В этих же условиях среды найдены и возможные восстановители углекислого газа. Восстанавливать его нужно, чтобы затем синтезировать органические вещества, ведь скелет каждой органической молекулы, в том числе аминокислот, углеводов, липидов, составляют атомы углерода, когда-то входившие в состав CO2.
В прошлом номере мы по составу неорганических ионов в живых клетках проследили их происхождение из вод геотермальных источников и грязевых котлов. В этих же условиях среды найдены и возможные восстановители углекислого газа. Восстанавливать его нужно, чтобы затем синтезировать органические вещества, ведь скелет каждой органической молекулы, в том числе аминокислот, углеводов, липидов, составляют атомы углерода, когда-то входившие в состав CO2.
Теория «железосерного мира» — первое развернутое описание, объединяющее восстановление CO2 с другими сторонами проблемы происхождения жизни, — принадлежит немецкому биофизику Гюнтеру Вахтерхойзеру («Philosophical Transactions of the Royal Society, B, Biological Science», 2006, 361, 1787—1806, doi: 10.1098/rstb.2006.1904, пересказ одной из предыдущих его статей на сайте «Элементы» — http://elementy.ru/ news/430373).
Вахтерхойзер обосновал теоретически и проверил экспериментально многие химические реакции, которые происходят в условиях, существующих вблизи «черных курильщиков» и древних континентальных горячих источников, — при температурах 50—150ОС и высоком давлении.
Основной источник восстановительных эквивалентов (то есть протонов, принимающих на себя электроны, которые необходимо перенести) — реакция сероводорода с сульфидом железа:
H2S + FeS → FeS2 + 2 [H].
Сульфид железа превращается в пирит, атомы водорода остаются адсорбированными на его поверхности. С помощью этих атомов водорода на поверхности сульфида железа может происходить фиксация азота:
N2 + 3 H2S + 3FeS 2 → NH3 + 3 FeS2,
восстановление CO2 до метилмеркаптана:
CO2 + 4H2S + 3FeS → CH3SH + 3 FeS2 + 2H2O,
восстановительное аминирование альфа-кетокислот:
R-CO-COOH + NH3 + FeS + H2S → R-CHNH2-COOH + FeS2 + H2O.
В присутствии сульфида никеля, также характерного для геотермальных источников, разнообразие химических продуктов сильно возрастает — CO2 и СО превращаются в уксусную, пировиноградную и другие органические кислоты, а также в тиометилацетат CH-CO-S-CH. Последний, реагируя с фосфорной кислотой, дает ацетилфосфат — высокоэнергетическое вещество, способное фосфорилировать органические молекулы, в том числе превращать АДФ в АТФ.
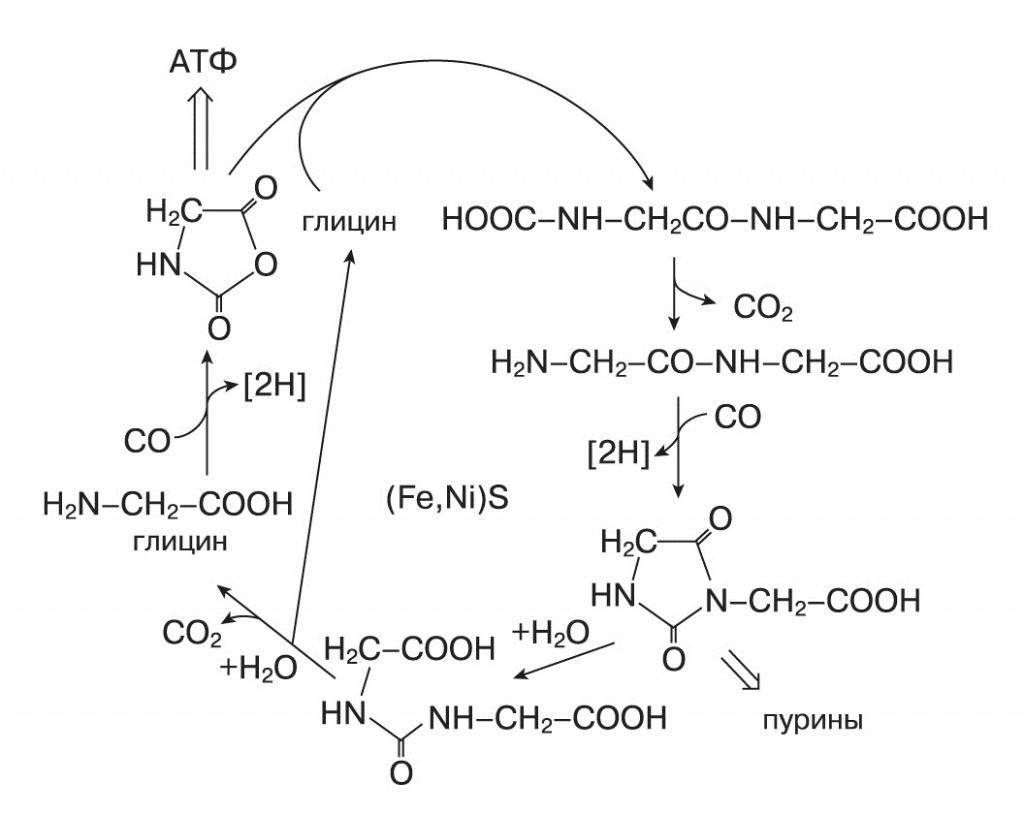
Отрицательно заряженные органические кислоты остаются адсорбированными на поверхности сульфидов и могут накапливаться в больших концентрациях. Там же происходят более сложные химические реакции, например пептидный цикл глицина, в котором образуются производные мочевины, гидантоины и пуриновые азотистые основания.
|
|
1. Дипептидный цикл глицина на FeS/NiS при высокой температуре (Wächtershäuser, 2006) |
В целом в условиях «черного курильщика» возможен синтез большого разнообразия органики, едва ли не больше, чем в опытах Миллера.
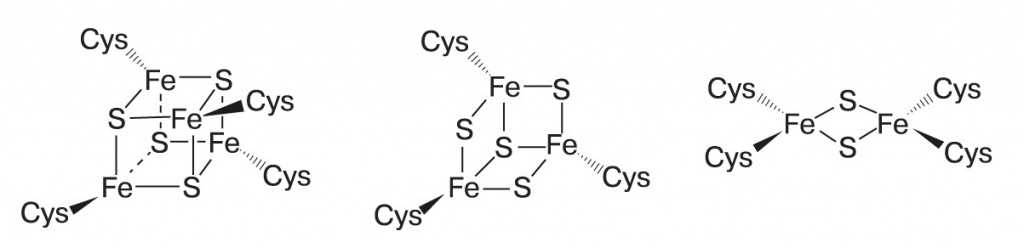
Дополнительный аргумент в пользу такого сценария — в ферментах современных клеток содержатся железосерные кластеры, фактически наночастицы пирита. Они переносят водород и участвуют в разнообразных окислительно-восстановительных реакциях. Особо сложный железосерный кластер находится в активном центре фермента нитрогеназы, который восстанавливает атмосферный азот до аммиака.
|
2. Структуры железосерных кластеров («Nature Chemical Biology», 2007, 3, 206—207, doi: 10.1038/nchembio0407-206) |
Другой сценарий абиогенного синтеза органики на геотермальных источниках — теорию «цинкового мира» — предложил Армен Мулкиджанян, о работах которого мы писали в предыдущей статье («Biology Direct», 2009, 4, 26, doi: 10.1186/1745-6150-4-26, Mulkidjanian, Galperin, «Biology Direct», 2009, 4, 27, doi: 10.1186/1745-6150-4-27). Он исходил из того, что сульфиды цинка и марганца способны к фотохимическому восстановлению разных веществ. Они, так же, как упомянутый в статье «Проблема хиральной чистоты» (2013, № 3) оксид титана TiO2, — полупроводники с широкой запрещенной зоной. Их кристаллы поглощают ближний ультрафиолет, и возбужденный электрон может оказаться в «потенциальной яме» на поверхности кристалла. В водной среде эти кристаллы восстанавливают CO2 до муравьиной кислоты и дикарбоновых кислот. Сульфид цинка оказывается самым эффективным восстановителем — с квантовым выходом до 80%. При этом на кристалле накапливается положительный заряд. Если нет подходящих восстановителей, то происходит фотокоррозия сульфида цинка с выходом ионов цинка в раствор и образованием молекулярной серы:
CO2+ZnS+H2O → (HCOO) 2Zn+Zn(OH)2+S.
Подобно сульфидам железа сульфид цинка на свету может восстанавливать азот до аммиака:
N2 + ZnS + H2O → NH3 + Zn(OH)2 + S,
который затем реагирует с муравьиной кислотой, давая формамид — ключевой промежуточный продукт для синтеза азотистых оснований. Восстановительное аминирование кетокислот в аминокислоты тоже хорошо катализируется сульфидом цинка при освещении.
Абиогенный фотосинтез на сульфиде цинка обладает еще некоторыми интересными свойствами. В роли восстановителя, предохраняющего ZnS от фотокоррозии, как оказалось, могут выступать восстановленные формы фосфора — фосфиты и гипофосфиты. В отличие от фосфатов, они хорошо растворимы в воде. В присутствии фосфитов ZnS проводит фотовосстановление CO2, сопряженное с окислением фосфита до фосфата. Фосфаты остаются адсорбированными на поверхности кристаллов, и это возможное объяснение высокой концентрации фосфатов в живых клетках. В некоторых условиях фотоокисление фосфита до фосфата на ZnS сопровождается фосфорилированием разных органических молекул и, возможно, полимеризацией нуклеозидов (сахар плюс азотистое основание) в полинуклеотиды.
Сульфид цинка хорошо адсорбирует нуклеиновые кислоты, так как шаг положительно заряженных ионов на его поверхности соответствует шагу фосфатов РНК и ДНК. Кроме того, сульфид цинка способен принимать фотовозбуждение с нуклеотидов, их полимеров, полипептидов и других молекул. С одной стороны, это защищает полимеры от УФ-расщепления, с другой стороны, накопление полимеров на поверхности минерала позволяет собирать больше света и ускоряет фотосинтез в этом месте — нуклеиновые кислоты работают подобно вспомогательным пигментам.
Теперь вернемся к восстановлению молекул углекислого газа. Подобно тому как минеральный состав цитоплазмы несет информацию о среде обитания самых первых клеток, современные пути восстановления CO2 живыми организмами могут воспроизводить какие-то древнейшие реакции, происходившие в неживых системах. Таких путей в современных клетках известно три.
Первый — цикл Кальвина, работающий в растениях и большинстве фотосинтезирующих и хемосинтезирующих бактерий. Когда школьникам говорят, что «растения поглощают углекислый газ и синтезируют глюкозу», речь идет именно о цикле Кальвина, но это сильно упрощенная правда (см. схему на следующей странице). Строго говоря, в цикле Кальвина синтезируется трехуглеродный фосфоглицериновый альдегид, а затем из него в несколько этапов получается глюкоза.
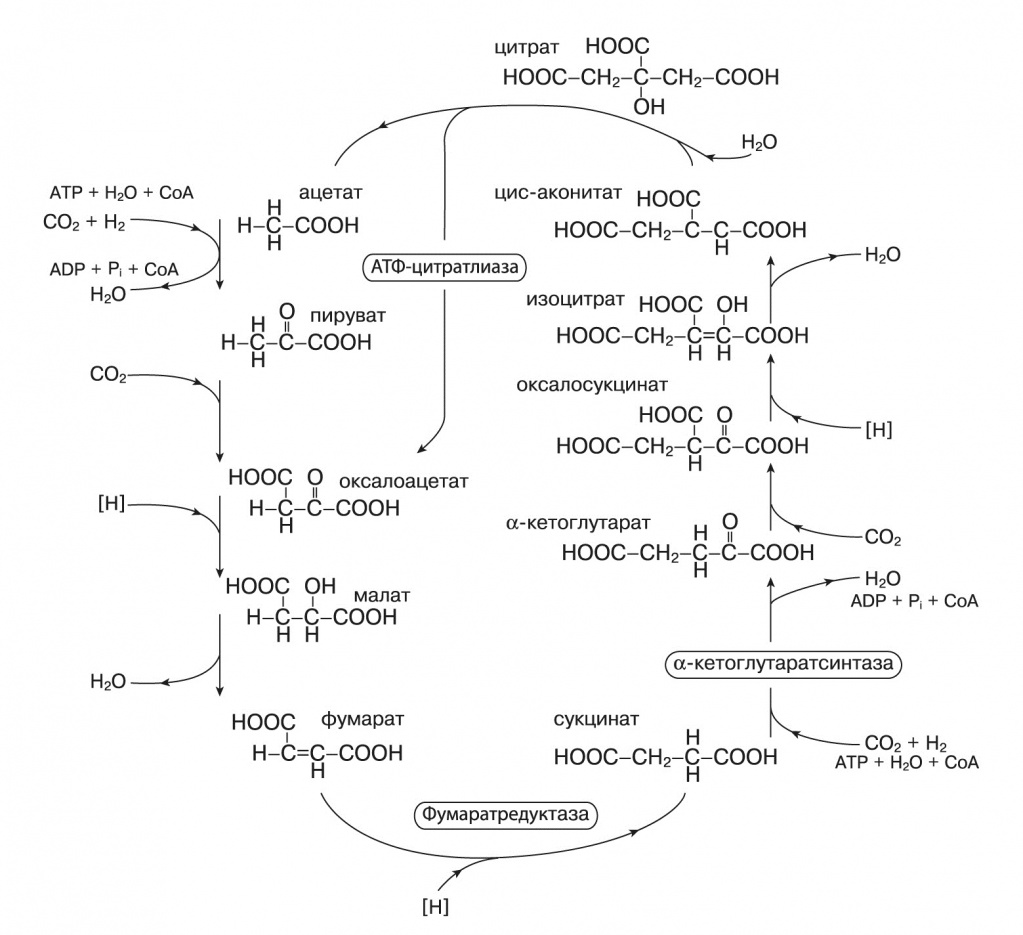
Второй — восстановительный цикл Кребса, работающий у некоторых анаэробных фотосинтезирующих бактерий. Выпускникам биологических факультетов хорошо известен обычный цикл Кребса, он же цитратный цикл или цикл трикарбоновых кислот, в котором двух- и трехуглеродные органические молекулы, образующиеся при распаде более крупных соединений, окисляются до CO2. Высвобожденные при этом протоны участвуют в синтезе АТФ, энергетической валюты клетки. Восстановительный цикл Кребса «вращается» в обратную сторону: поглощаются молекулы CO2 и протоны на носителе, затрачивается энергия АТФ, образуется четырехуглеродная щавелевоуксусная кислота (оксалоацетат). Заметим, что протоны переносит не кофермент NADH, как в обычном цикле Кребса, а ферредоксин — железосерный белок с высоким восстановительным потенциалом.
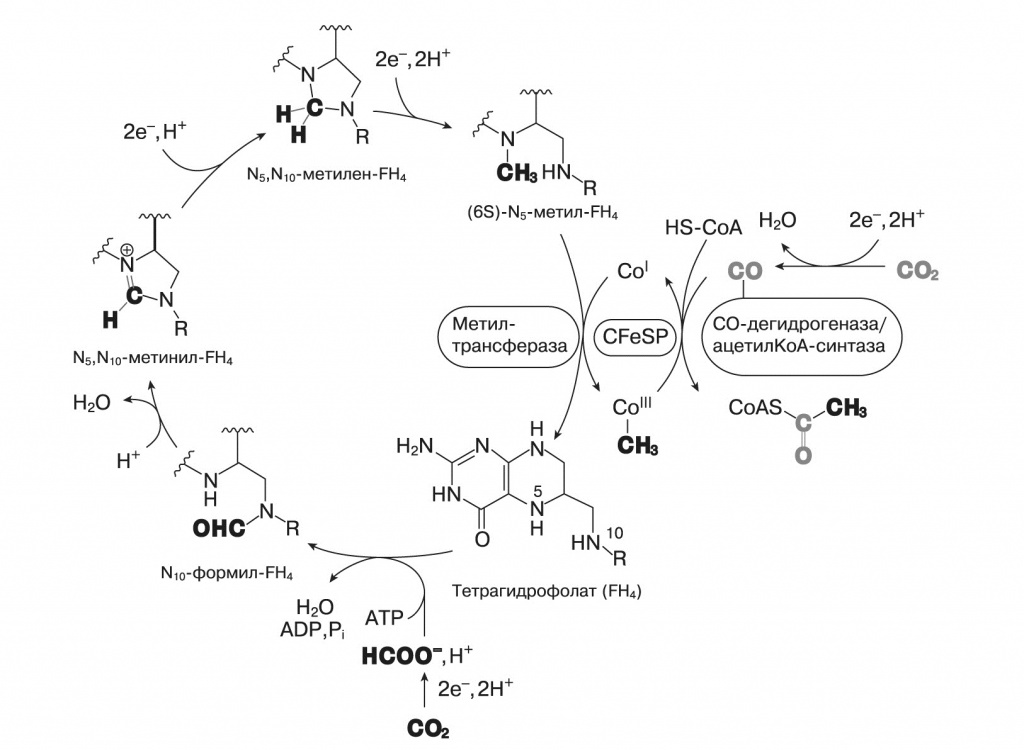
Третий — восстановительный ацетил-КоА-путь, который имеется у некоторых хемосинтезирующих бактерий и архей. Кофермент А, или КоА, участвует во многих важных биохимических процессах (в том числе и в цикле Кребса, и в цикле Кальвина). Его задача — переносить остатки органических кислот на другие молекулы, например, если с коферментом связан ацетат, это соединение и называют «ацетил-КоА». Восстановительный ацетил-КоА-путь включает в себя параллельное восстановление двух молекул CO2: одна окисляется до СО, другая — до связанной с коферментом метильной группы. Потом они соединяются и переносятся на кофермент А. Возможная роль этой реакции в предбиогенной химии рассмотрена в статье Уильяма Мартина и Майкла Расселла («Philosophical Transactions of the Royal Society, B, Biological Science», 2007, 362, 1887—1925, doi: 10.1098/rstb.2006.1881).
Попробуем оценить возможность протекания этих реакций без ферментов, с участием минеральных катализаторов.
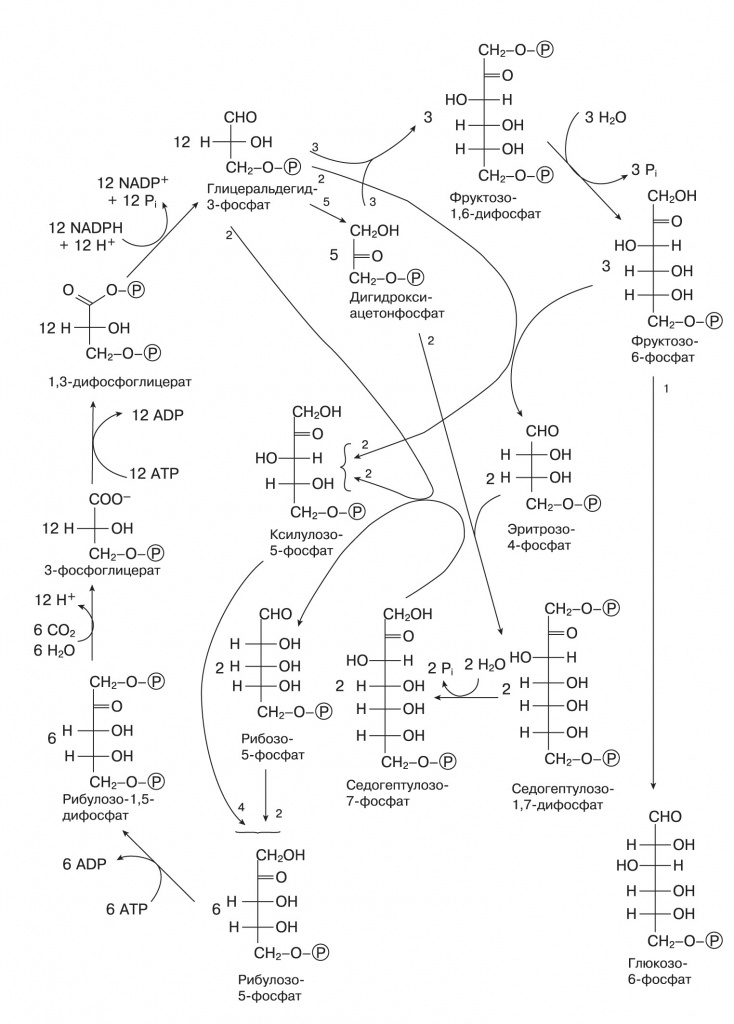
| 3. Цикл Кальвина |
|
| 4. Восстановительный цикл Кребса |
|
|
5. Восстановительный ацетил-КоА-путь фиксации СО2. Выделены группы, содержащие атомы углерода из двух молекул углекислого газа. В итоге они образуют ацетат, присоединенный к коферменту А. CFeSP — белок, содержащий железосерные кластеры |
Если посмотреть на состав ферментов, катализирующих эти реакции, то бросается в глаза единообразие каталитических металлов в активных центрах. Все реакции восстановительного цикла Кребса катализируются атомами железа, кроме одной, где участвует марганец. В цикле Кальвина в качестве катализаторов используются ионы магния и иногда цинка, так что для любого из трех путей можно допустить, что он катализируется поверхностями одного-двух минералов.
На первый взгляд, хороший претендент на роль предбиологического пути восстановления CO2 и предшественника биохимии — восстановительный цикл Кребса. Он, как и его более привычный окислительный аналог, находится в центре всего метаболизма. Из его промежуточных продуктов начинаются все основные пути синтеза — аминокислот, липидов, сахаров, пирролов, пиримидиновых азотистых оснований («Proceedings of the National Academy of Sciences USA», 2000, 97, 14, doi: 10.1073/ pnas.110153997). Этот цикл — автокаталитический, то есть может производить собственные промежуточные продукты и повышать производительность. Однако есть и возражения, подробно рассмотренные в статье Лесли Оргела («PLoS Biology», 2008, 6, doi: 10.1371/journal.pbio.0060018), и главное из них — проблемы со специфичностью минерального катализа. Если у нас есть минерал, катализирующий восстановление альфа-кетокислот до гидроксикислот, например оксалоацетата до малата, то он должен также восстанавливать пируват до молочной кислоты и альфа-кетоглутарат до альфа-гидроксиглутарата, которые уже не входят в этот цикл реакций. Аналогичным образом минеральный катализатор распада цитрата, скорее всего, будет расщеплять и другие кислоты этого цикла.
Цикл Кальвина выглядит очень сложным. Однако в нем есть лишь один шаг включения CO2 в органику и один шаг восстановления (от рибулозо-1,5-дифосфата до глицеральдегид-3-фосфата), тогда как в восстановительном цикле Кребса — четыре включения CO2 в разные вещества и четыре шага восстановления. Все остальные реакции цикла Кальвина — просто перестройки сахаров, они полностью аналогичны реакции Бутлерова. Следовательно, для их протекания может быть достаточно одного минерального катализатора, специфично адсорбирующего рибулозодифосфат или просто рибулозу и направляющего таким образом реакции к одному продукту. С другой стороны, цикл Кальвина далек от большинства биохимических путей, он соединяется с ними только через сахара и цикл Кребса. Но для синтеза нуклеотидов и РНК нужны именно сахара, и у некоторых архебактерий известен вариант цикла Кальвина, который начинается не с рибулозодифосфата, а с остатка рибозы в составе аденинового нуклеотида.
Восстановительный ацетил-КоА-путь несложен и дает на выходе ацетил- КоА, универсальный промежуточный метаболит, но требует разнообразных катализаторов: помимо ионов металлов (железо, никель, кобальт, молибден и вольфрам), для него нужны сложные органические коферменты — тетрагидрометаноптерин либо тетрагидрофолиевая кислота. Кроме того, он не является автокаталитическим и не может наращивать собственную продуктивность.
Итак, ни один из трех современных путей фиксации CO2 нельзя прямо представить в роли предбиологического механизма синтеза органики. Возможно, однако, что эти пути выделились путем упорядочения и упрощения более сложной сети реакций, которая как-то утилизировала и возвращала в автокаталитический цикл продукты побочных реакций (в случае восстановительного цикла Кребса) или давала неизвестные ныне связи синтеза сахаров с другими метаболическими путями для цикла Кальвина. На сегодня экспериментально удалось только провести часть реакций восстановительного цикла Кребса на суспензии сульфида цинка.
Теория «цинкового мира» предсказывает, что цитоплазма клеток, РНК-структуры и белки должны быть обогащены ионами цинка. Как мы видели в предыдущем номере, цинк по содержанию в цитоплазме сравним с железом и превосходит все прочие переходные металлы. В структурах РНК железо совершенно отсутствует, а цинк встречается чаще других переходных металлов. За ним следуют марганец, кобальт и вольфрам.
Многие рибозимы (молекулы РНК, обладающие каталитической активностью подобно ферментам-белкам) активны только в присутствии ионов металлов. Среди таких металлов самые распространенные — магний, цинк и марганец, а железо никогда не встречается.
Цинком также обогащены самые древние белки и ферменты с древними функциями. Из 49 универсальных белковых третичных структур (таких, которые присутствовали во всех прочитанных на 2008 год геномах), 37 содержат цинк, 19 — марганец и только 3 — железо. При этом цинк не обязательно нужен для каталитической активности, часто он просто стабилизирует трехмерную структуру. Одна из таких древних структур — ДНК-РНК-связывающий домен под названием «цинковый палец», где атом цинка связан двумя остатками цистеина и двумя — гистидина, очень часто встречается, например, в белках — факторах транскрипции.
Среди активных центров ферментов цинк и марганец преобладают в лиазах, трансферазах и гидролазах, тогда как железо и медь, в том числе похожие на пирит железосерные кластеры, — в более эволюционно молодых окислительно-восстановительных ферментах, медь — практически только в ферментах, работающих с молекулярным кислородом. Таким образом, можно сказать, что содержание металлов в клетках подтверждает теорию «цинкового мира», а не «железосерного мира».
В пользу цинкового мира говорит еще то обстоятельство, что ионы железа эффективно гидролизуют РНК, связываясь с гидроксильными группами рибозы. Вахтерхойзер, чтобы обойти эту сложность, говорит, что первые нуклеиновые кислоты содержали вместо рибозы четырехуглеродные сахара, например эритрозу. Такие нуклеиновые кислоты были получены искусственно, они устойчивы к ионам железа, щелочам и высокой температуре и могут комплементарно соединяться с классическими РНК, но в таком случае непонятно, почему они сменились более уязвимыми нуклеиновыми кислотами с рибозой.
В целом теория «цинкового мира» находит больше подтверждений, однако полностью отвергать роль химических реакций на поверхности пирита нельзя. В конце концов, зоны сульфидов железа и сульфидов цинка соседствуют в одних и тех же «черных курильщиках». Вещества, синтезируемые на сульфиде железа, постепенно смываются и переносятся с током воды и пара в зону сульфида цинка, где могут включаться в происходящие там под действием света процессы. Одним из важных для будущей биохимии веществ мог быть тиометилацетат — простой органический аналог ацетилкофермента А, способный легко переносить ацетильную группу на другие органические молекулы.
Элементы жизни: почему не кремний и не фтор
Фотохимия и «черные курильщики»
Пути восстановления углекислого газа
Происхождение белкового синтеза и генетического кода
Мир вирусов, последний общий предок и происхождение ДНК
Происхождение мембран и мембранной биоэнергетики
Закат «цинкового мира», прокариотная биосфера и происхождение фотосинтеза