Технеций: что нового
Поводов для написания этой статьи было несколько. Во-первых, последний раз статья о технеции была опубликована в журнале почти 40 лет назад – в январе 1970 года. С тех пор очень многое изменилось. Во-вторых, в мае 2008 года на химическом факультете МГУ состоялось празднование ежегодного, 43-го по счету, Дня химика, который был посвящен очередному химическому элементу. Под номером 43 в периодической таблице значится технеций, символ которого и фигурирует на выпущенных к празднику значках (рис. 1). Наконец, автор решил, в лучших традициях исследователей прошлого, испытать на себе применение этого элемента в биохимических и медицинских исследованиях.
 |
|
1. Значки, выпущенные к празднику |
Хевеши и радиоактивные индикаторы
Нобелевская премия по химии за 1943 год была присуждена венгру Дьёрдю Йожефу фон Хевеши (в другом написании – Георгу де Хевеши) «за работы по использованию изотопов в качестве индикаторов при изучении химических процессов». О присуждении было объявлено 9 ноября 1943 года, но лишь 10 декабря 1944 года с традиционной речью выступил председатель Нобелевского комитета по химии профессор Арне Вестгрен. Еще одна особенность военного времени: Вестгрен представил работу Хевеши не на торжественной церемонии, а по радио. В своей речи он сказал следующее (сокращенный перевод с сайта Нобелевского комитета www.nobelprize.org, примечания автора в скобках):
«В 1913 году молодой исследователь де Хевеши, работая в лаборатории Резерфорда в Манчестере, получил задание отделить радий D от радиоактивного свинца. Хевеши не удалось это сделать. Фактически стало очевидно, что радиоактивный радий D настолько незначительно отличается от неактивного радия G (последнего из дочерних элементов в ряду распада радия), что все попытки отделить их друг от друга были, по-видимому, обречены на неудачу. (Радий G и радий D – старые радиохимические обозначения двух изотопов свинца, соответственно стабильного 206Pb и радиоактивного 210Pb с периодом полураспада около 22 лет.) Хотя Хевеши не удалось разделить указанные изотопы, его работа не была напрасной. Она привела его к идее о новом методе исследования в химии. Поскольку химически невозможно отделить радиоактивный изотоп от его стабильного аналога, появляется возможность использовать это его свойство, чтобы детально проследить за поведением данного элемента в ходе различных химических реакций и физических процессов.
Используя в качестве маркера радий D, де Хевеши определил растворимость ряда соединений свинца, обладающих крайне малой растворимостью. Ему удалось также изучить процесс самодиффузии в металле; до него количественно изучать подобные процессы было невозможно. Хевеши осаждал торий В (212Pb, период полураспада 10,6 ч) на поверхность свинцового кристалла и затем следил за снижением интенсивности излучения, вызванного проникновением радиоактивных атомов с поверхности в глубь кристаллической решетки, при этом их место занимали неактивные атомы из более глубоких слоев. Таким способом он смог измерить энергию, необходимую для извлечения атома из кристалла свинца, то есть энергию диссоциации кристаллической решетки. Оказалось, что эта энергия имеет тот же порядок величины, что теплота испарения свинца (194 и 195,1 кДж/моль соответственно).
Новый метод оказался также пригоден для изучения биологических процессов. Бобы, помещенные в растворы, содержащие соли свинца с примесью атомов радиоактивного свинца, частично поглощали эти соли. При этом свинец, который является для растений ядом и препятствует их нормальному развитию, по-разному накапливался в разных частях растения. Хевеши изучил также поглощение и выделение солей свинца, висмута и таллия организмами животных. Знать, как распределяются соединения висмута, введенные в организм животного, важно для медицины, поскольку, как известно, некоторые соединения висмута используются в терапевтических целях.
В качестве маркеров вначале использовали только природные радиоактивные элементы, и это неизбежно ограничивало применение нового метода. Фактически его можно было использовать только для тяжелых металлов – свинца, тория, висмута, таллия и их соединений. Ситуация должна была в корне измениться после работ Фредерика и Ирен Жолио-Кюри, а также Ферми, которые сумели получить искусственные радиоактивные изотопы многих элементов. С тех пор исследование химических процессов с помощью радиоактивных индикаторов было значительно усовершенствовано и используется в лабораториях всего мира.
Исключительно важные результаты были получены при использовании этого метода в биологии. Здесь главным образом используется радиоактивный изотоп фосфора 32 Р. Для биологических исследований он имеет достаточно большое время жизни: его период полураспада составляет 14,3 суток. Хевеши готовил физиологические растворы фосфата натрия, содержащие этот маркер, и вводил их в организм животных и людей. Через определенные промежутки времени он определял, каким образом фосфор распределяется в организме. Исследование образцов крови показало, что фосфор, введенный в кровь, быстро из нее выводится. В крови человека содержание радиоактивного фосфора уже через два часа снижается до 2% от исходного уровня. Он диффундирует во внеклеточную жидкость и постепенно замещает атомы фосфора в тканях, органах и костях скелета. Спустя определенное время радиоактивный фосфор можно обнаружить, хотя и в очень малых количествах, даже в зубной эмали.
Со времени работ Хевеши изменилось очень многое. Впервые радиоактивную метку использовали в медицинских целях в конце 1930-х годов, когда человеку ввели препарат меченого иода и затем с помощью счетчика Гейгера определили, какая его доля сконцентрировалась в щитовидной железе. В 1948 году был разработан метод регистрации γ-излучения с использованием фотоумножителей. В 1962 году создана так называемая гамма-камера (камера Анжера) – сцинтилляционная счетная камера для регистрации излучения. Сцинтилляция (от лат. scintillo – блистать, сверкать) – вспышка света, возникающая в некоторых жидких или твердых веществах под действием ионизирующих излучений. Это позволило получить изображение железы с разрешением 400 точек на дюйм, при времени сканирования более 1,5 часов. Вскоре стало возможно исследовать и другие органы. Одновременно росла точность регистрации γ-излучения. В 70-е годы к гамма-камерам были подключены компьютеры, это радикально улучшило обработку информации и построение изображений. Так появилась однофотонная эмиссионная компьютерная томография, она же гамма-томография (англ. SPECT – single-photon emission computed tomography). Название «однофотонная» означает, что при каждом акте радиоактивного превращения эмитируется один гамма-квант. Вторая революция произошла, когда для диагностики стали использовать один из изотопов технеция.
Технеций и его свойства
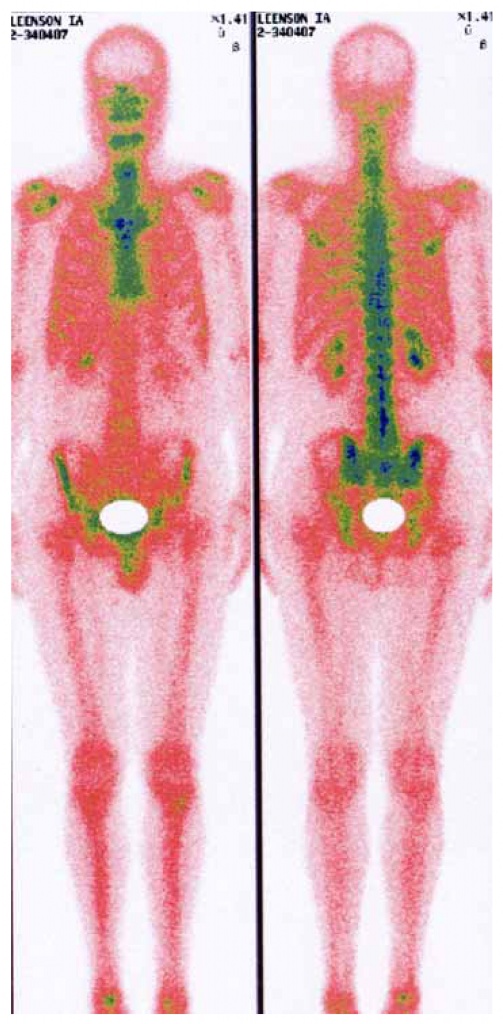 |
Портрет в лучах технеция |
Технеций был открыт, вернее, синтезирован и идентифицирован по его радиоактивности в 1937 году. Это был первый в истории химический элемент, полученный в лаборатории, а не найденный в природе, его название происходит от греч. τεχνη – ремесло, искусство, умение; τεχνητος – искусственный. Того же происхождения и слово «техника», что и отразили дизайнеры значка, посвященного технецию.
Существование элемента с атомным номером 43 предсказал Д.И.Менделеев, дав ему условное название «экамарганец», то есть «первый аналог марганца». В современной периодической таблице (как в короткой, так и в длинной ее форме) технеций расположен в седьмой группе между марганцем и рением. Неизвестный при жизни Менделеева рений он назвал, также используя санскритские числительные, «вторым аналогом марганца» – «двимарганцем». Рений оказался последним химическим элементом, впервые выделенным из природного источника. Это случилось в 1925 году, до открытия технеция. Попытки обнаружить в минералах технеций оказались безуспешными, хотя многие исследователи заявляли, что им это удалось. Вряд ли можно найти другой элемент, имеющий столько «ложных предшественников»: клетка периодической таблицы с номером 43 последовательно «заполнялась» ильмением, девием, люцием, ниппонием, мазурием.
Впервые следовые количества технеция были идентифицированы в Италии – физиком Эмилио Сегре и химиком Карло Перье, работавшими тогда на физическом факультете университета Палермо. Новый элемент был получен в результате бомбардировки молибдена дейтронами с энергией 5 МэВ на одном из первых циклотронов (диаметром всего 70 см) Эрнеста Лоуренса в Радиационной лаборатории Калифорнийского университета. Это не был заранее спланированный эксперимент: Сегре, который летом 1936 года посетил с женой США, упросил Лоуренса отдать ему для исследований облученную молибденовую фольгу – часть отражателя циклотрона (его назначение – выводить ускоренный пучок ионов наружу). И в начале 1937 года Лоуренс отправил эту фольгу в Палермо.
Молибден – сосед технеция по периодической таблице, его порядковый номер 42. И если ядро одного из стабильных изотопов молибдена захватит ядро дейтерия, заряд ядра увеличится на единицу, то есть оно превратится в ядро элемента 43. Стабилизация ядра происходит путем выброса одного или двух нейтронов. Соответственно образовавшееся ядро технеция будет иметь массу на единицу меньше, чем у исходного молибдена, или такую же, например: 92Мо + 2Н → 93Тс + n; 92Мо + 2Н → 92Тс + 2n. Трудности отделения нового элемента от всех возможных примесей подробно описаны в статье В.И.Кузнецова («Химия и жизнь», 1970, № 1). Исследователи зафиксировали новые радионуклиды по их периодам полураспада. В последующем оказалось, что это были 95Tc и 97Tc. После открытия Сегре вернулся в Беркли, разыскал работавшего в Калифорнийском университете молодого и пока незнаменитого Гленна Сиборга, и в совместной работе они выделили еще один изотоп, метастабильный технеций-99m.
Впервые весовые количества технеция были получены в США во второй половине 40-х годов в результате облучения 5,7 кг молибдена нейтронами в ядерном реакторе. Его отделили от молибдена, используя летучесть оксида Тс2О7. Образуется технеций также при облучении рутения (44) и ниобия (41). В настоящее время технеций в основном выделяют из смеси продуктов деления урана-235 в отработанном ядерном топливе. Больше всего получается технеция-99, 101, 102 и 103 (соответственно 6,1, 5,6, 4,3 и 3% относительно всех продуктов деления). При полном распаде 1 г 235U образуется 27 мг 99Тс. В реакторе мощностью 285 МВт ежедневно образуется 8 г технеция, то есть 3 кг в год. Технеций получается также при делении ядер 233U и 239Pu. Всего таким способом образовалось уже свыше 100 тонн технеция. Конечно, его еще нужно отделить от других продуктов деления и очистить. В 2005 году этот элемент продавали по 83 доллара за грамм. Миллиграммовые количества технеция получают путем длительного облучения нейтронами молибдена высокой степени чистоты: 98Mo + n → 99Mo → 99mTc → 99Tc → 99Ru + e. Так, при двухмесячном облучении 1 кг МоО3 в реакторе потоком нейтронов плотностью 1014 /(см2 с) образуется 10–15 мг 99Тс. Довольно много технеция, порядка 1,5 т, уже попало (и продолжает попадать) в окружающую среду. Это происходит в основном при переработке ядерного топлива и в результате ядерных испытаний. Исчезнет этот технеций только через десятки миллионов лет.
В настоящее время известно 56 изотопов технеция (включая ядерные изомеры) с массой от 85 до 118 и периодами полураспада от долей микросекунды до миллионов лет. Напомним, что у ядерного изомера атомное ядро находится в возбужденном (метастабильном) состоянии и потому рано или поздно переходит в основное состояние с выделением энергии. Такие изомеры могут образовываться при делении ядра на осколки или в других ядерных реакциях. Ядерные изомеры (их обозначают буквой m, а если изомеров несколько – m1, m2 и т. д.) имеют собственное время жизни – как у любого другого радионуклида. Обычно такие изомеры неустойчивы и переходят в основное состояние за доли пикосекунды, как правило, с выделением гамма-квантов. Однако если спин возбужденного состояния сильно отличается от спина основного состояния ядра, переход оказывается запрещенным и происходит медленно. Иногда изомер бывает даже стабильнее, чем его основное состояние, причем различие может быть очень большим. Так, у 108Ag (спин ядра 1) период полураспада 2,37 мин., а у его изомера 108mAg (спин ядра 6) – 127 лет!
Самые долгоживущие изотопы технеция – 98Тс (период полураспада 4,2 млн. лет), 97Тс (2,6 млн. лет) и 99Тс (211 тыс. лет). Это значительно меньше времени жизни Земли, поэтому технеций в природе встречается лишь в виде следов в урановых рудах как продукт спонтанного деления урана. По оценкам, сделанным в Лос-Аламосской лаборатории, 1 кг урана содержит около 1 нг технеция – триллионную часть. Впервые его удалось обнаружить в природе в 1962 году в урановой смолке из Бельгийского Конго; это был 99Тс, образовавшийся в результате спонтанного деления ядер урана-238. Довольно много технеция-99 образовалось миллионы лет назад при работе африканского природного ядерного реактора («реактора Окло») на территории современного Габона. Но с тех пор он практически исчез в результате распада: 99Тс → 99Ru + e. В 1954 году ничтожные следы технеция были найдены в некоторых молибденовых минералах.
В 1952 году астроном Пол Меррил обнаружил в спектрах некоторых звезд – красных гигантов – линии при 403,1 нм, 423,8 нм, 426,8 нм и 429,7 нм. Это линии в спектре технеция, который накапливается в этих массивных звездах к концу их жизни. Впоследствии выяснили, что технеций образуется в оболочках красных гигантов в результате так называемого s-процесса (от англ. slow – медленный) – захвата ядрами нейтронов.
У изомера 99mТс наблюдается редкий случай изменения, хотя и незначительного, периода полураспада в зависимостиот условий. Так, в составе соединения КТсО4 этот период уменьшается на 1 с, а в составе Тс2S7 – на 8,6 с по сравнению с «голым» нуклидом, то есть на 0,04%. Влияют на время жизни этого изомера также температура и давление.
Легкие изотопы технеция распадаются преимущественно с испусканием позитрона или путем захвата орбитального электрона. Тяжелые изотопы претерпевают в основном бета-распад. Почти все радиоактивные превращения изотопов технеция сопровождаются гамма-излучением. Но есть и исключения. Так, 99Тс – самый распространенный изотоп технеция – можно использовать как источник чистого бета-излучения с небольшой энергией 292 кэВ; оно задерживается уже стеклянными стенками лабораторной посуды. Для сравнения: энергия β-частиц, испускаемых 98Тс, – 4,0 МэВ. Наиболее опасно при работе с технецием, как и с другими радионуклидами, вдыхание мельчайших капелек растворов или пыли твердых реагентов.
Большое время жизни основных изотопов технеция позволило хорошо изучить свойства этого элемента. Технеций – тугоплавкий (температура плавления 2200°С) серебристо-серый металл, несколько тяжелее свинца (плотность 11,5 г/см3). Во влажном воздухе постепенно тускнеет. Он растворяется в азотной и концентрированной серной кислотах, соляная кислота на него не действует. По химическим свойствам технеций – аналог марганца и рения, больше похожий на рений, может проявлять степени окисления от –1 до 7. Получено и исследовано множество соединений технеция – оксиды (ТсО2, ТсО3 и Тс2О7), галогениды и оксогалогениды (TcF5, TcF6, TcCl4, TcCl6, ТсОСl3, TcOBr3, TcOCl4, TcO3F, TcO2F3 и др.), галогенотехнетаты (NaTcF6,K2TcCl6 и др.), сульфиды (ТсS, TcS2, Tc2S7), карбонилы (Тс2(СО)8, Тс2(СО)10), комплексные и кластерные соединения (К2[Тс(CN)6 ], Тс4(СО)12F(ОН)3, аналог ферроцена [Тс(С5Н5)2]2 и другие). П.А.Козьмин с соавторами в Институте общей и неорганической химии РАН получили необычные структуры многоатомных кластеров технеция.
Если технеций сжечь в чистом кислороде при 500°С, получается желтый кристаллический оксид Тс2О7, плавящийся при 120°С с образованием вязкой жидкости, которая кипит без разложения при 311°С. Удивительный факт: твердый Тс2О7 проводит электрический ток, а жидкий – нет (Re2О7 в этом отношении ведет себя «правильно»). И еще одно необычное свойство этого оксида: он не окисляет органические вещества (Mn2О7 реагирует с ними со взрывом!). При упаривании водного раствора Тс2О7 выделяются темно-красные кристаллы технециевой кислоты НТсО4. Ее водные растворы тоже обладают необычным свойством: концентрированные растворы красные, разбавленные – бесцветные. В отличие от перманганатов, соли технециевой кислоты (пертехнетаты) бесцветны и очень устойчивы. Так, КТсО4 плавится при 540°С и возгоняется при 1000°С без разложения (КМnО4 разлагается уже при 250°С). При термическом разложении NH4ТсО4 образуется нелетучий черный диоксид ТсО2. Пертехнетаты оказались превосходными ингибиторами коррозии, если бы не были дорогими и радиоактивными. То же можно сказать и об исключительно активных технециевых катализаторах. Так, они могут в десятки раз повысить выход аммиака при его синтезе из водорода и азота. В реакции дегидрирования изопропилового спирта они намного превосходят по эффективности палладий или рутений.
Технеций в медицине
В 1961 году пертехнетат-анион 99mТсО42– впервые применили в медицинских целях – для диагностирования заболевания щитовидной железы. Впоследствии химия технеция была подробно изучена с целью применения этого элемента в ядерной медицине. Несомненный лидер здесь – изомерный радионуклид 99mТс, используемый в более чем 85% всех анализов для диагностики множества заболеваний, в том числе онкологических. В настоящее время во всем мире с помощью 99mТс ежегодно проводят свыше 20 миллионов таких исследований. Этот радионуклид имеет массу преимуществ. Во-первых, он практически на 100% претерпевает единственный переход 99mТс → 99Тс. При этом испускаются гамма-кванты. Их энергия 0,14 МэВ, она близка к энергии рентгеновского излучения, которое используют в целях диагностики и которое удобно регистрировать. Но, в отличие от рентгенографии, в данном случае источник радиации расположен внутри тела.
Во-вторых, 99mТс достаточно просто получить, и он обладает очень удобным для диагностики периодом полураспада – 6,04 часа. За это время легко не только провести практически любое исследование, но и приготовить подходящий для данного случая радиофармацевтический препарат. А уже через сутки от исходного количества радионуклида остается всего одна восьмая.
Третье важное преимущество заключается в том, что основное состояние, в которое переходит 99mТс, то есть 99Тс, имеет весьма большой период полураспада – более 200 тысяч лет. Значит, активность исходного препарата после его распада снижается более чем в 300 млн. раз. В результате и исходный 99mТс, и тем более дочерний 99Тс нанесут минимальный вред человеку. Вдобавок они выводятся из организма за несколько дней.
В настоящее время ядерная медицина только в США имеет оборот более 10 миллиардов долларов, а ядерно-медицинские процедуры проводятся более 50 пациентам на 1000 населения в год (в РФ на порядок меньше). Радиофармпрепаратов известно несколько десятков, и они применяются для самых разнообразных исследований мозга, сердца, щитовидной железы, легких, печени и желчного пузыря, почек и надпочечников, костей скелета, крови, а также для диагностики опухолей. В последнем случае используют, например, метод иммуносцинтиграфии: 99mТс вводят в моноклональное антитело – белок иммунной системы, способный связываться с раковыми клетками. Через несколько часов после инъекции препарата регистрируют гамма-излучение из различных точек организма и строится компьютерное изображение. Область высокой интенсивности излучения указывает на место расположения опухоли. Если ввести 99mТс в некоторые препараты олова, этот радионуклид окажется связанным с эритроцитами. В результате появится возможность выявить нарушения в системе кровообращения. А в составе коллоидной серы 99mТс улавливается мононуклеарными фагоцитами и концентрируется в основном в печени (в небольшой степени – в селезенке).
Откуда медики берут 99mТс, время жизни которого составляет считанные часы? Заранее его не запасешь, ядерный реактор или ускоритель в клинике не поставишь. Он непрерывно образуется из радиоактивного молибдена-99: 99Мо → 99mТс + е. Сам же 99Мо несложно получить путем облучения в ядерном реакторе нейтронами стабильного 98 Мо, которого в природном молибдене 24,1%. Правда, и молибден-99 живет не слишком долго: период его полураспада 66 часов. Но этого достаточно, чтобы доставить так называемый генератор технеция (рис. 2) в клинику и там в течение нескольких дней «выдаивать» из него по мере необходимости требуемое количество 99mТс. Действительно, десятикратная потеря активности 99Мо происходит в течение 220 часов, так что работать с ним можно по крайней мере в течение недели и получить примерно 10 препаратов. Сравнительно небольшое время жизни 99Мо имеет и свои преимущества: 99mТс образуется из него достаточно быстро. При этом по мере накопления 99mТс его можно отделять от молибдена. Интересно, что в английском языке для процессов, подобных этому, используются термины «cow» – корова (в данном случае это будет «molybdenum cow») и to milk – доить. Активность, исходящая из генератора, настолько мала, что подобный эксперимент был недавно предложен даже в качестве практической работы в курсе химии для американских студентов.
 |
|
2. Генератор 99mТс; потребность в подобных генераторах в РФ – более 4000 в год
|
В генераторе непрерывно идут превращения 99Мо → 99mТс → 99Тс. Распадом последнего за время эксперимента можно пренебречь. Это — типичная последовательная реакция, причем константа скорости первой стадии в 11 раз больше второй. При достаточно большой разности в константах распада наступает так называемое радиоактивное равновесие: концентрация второго вещества убывает в такой же степени, в которой расходуется исходное вещество. Поэтому в течение нескольких часов количество 99mТс в генераторе остается почти постоянным. На практике в хроматографическую колонку с оксидом алюминия помещают очищенный неактивный 98Мо. Алюминий очень слабо поглощает нейтроны, поэтому колонку можно прямо облучать нейтронами, превращая некоторое количество молибдена-98 в его радиоактивный изотоп 99Мо. Радиомолибден (обычно в виде молибдата) превращается в технеций-99m с испусканием β-частиц: 99Мо → 99mТс + е.
Отделить образовавшийся технеций от молибдена можно разными способами. Один из них состоит в экстракции 99mТс ацетоном или метилэтилкетоном из щелочного раствора молибдата. Если молибден был адсорбирован на Аl2О3 из азотнокислого раствора, то для отделения 99mТс колонку промывают разбавленной азотной кислотой. В клиниках пертехнетат-анион 99mТсО42– извлекают из колонки с помощью стерильного физиологического раствора. По своим свойствам пертехнетат значительно отличается от молибдата и легко вымывается из колонки. В любом случае «проскок» молибдена должен быть сведен к минимуму (по федеральному закону США активность 99Мо в элюате не должна превышать 0,015% от активности 99mТс). Далее из пертехнетата можно получить самые разнообразные препараты; времени жизни 99mТс для этого достаточно.
Отмеченное выше разнообразие химии технеция весьма пригодилось при синтезе разнообразных фармпрепаратов, содержащих этот элемент и используемых в медицинской диагностике. Технеций способен образовывать прочные комплексы (типа хелатов) с самыми разнообразными соединениями. Реакция идет быстро: достаточно добавить элюированный из колонки пертехнетат к соответствующему препарату. Такие препараты синтезируются на фармацевтических фабриках и поставляются в стерильных флаконах. При их контакте с пертехнетатом последний, как правило, восстанавливается – до Тс(I), Tc(III), Tc(IV) или Tc(V).
В диагностике используются препараты технеция двух типов: простые молекулы, в которых атомы Тс составляют неотъемлемую часть и без которых соединение не будет концентрироваться в нужном месте, либо сложные органические молекулы – антитела, белки, гормоны, меченые атомами технеция. Для этого используют, например, мультидентатный лиганд, в котором одни группы координационно связываются с атомом Тc, а другие образуют ковалентные связи со сложной молекулой.
Одними из первых были синтезированы препараты Тс(IV), которые давали изображения костей. В них атомы Тс координационно связаны с различными алкилдифосфонатами, например с гидроксиметилендифосфонатом. Такие препараты аккумулируются прежде всего в местах активного роста костей (например, при переломах). Структуры некоторых широко применяемых препаратов показаны на рис. 3.
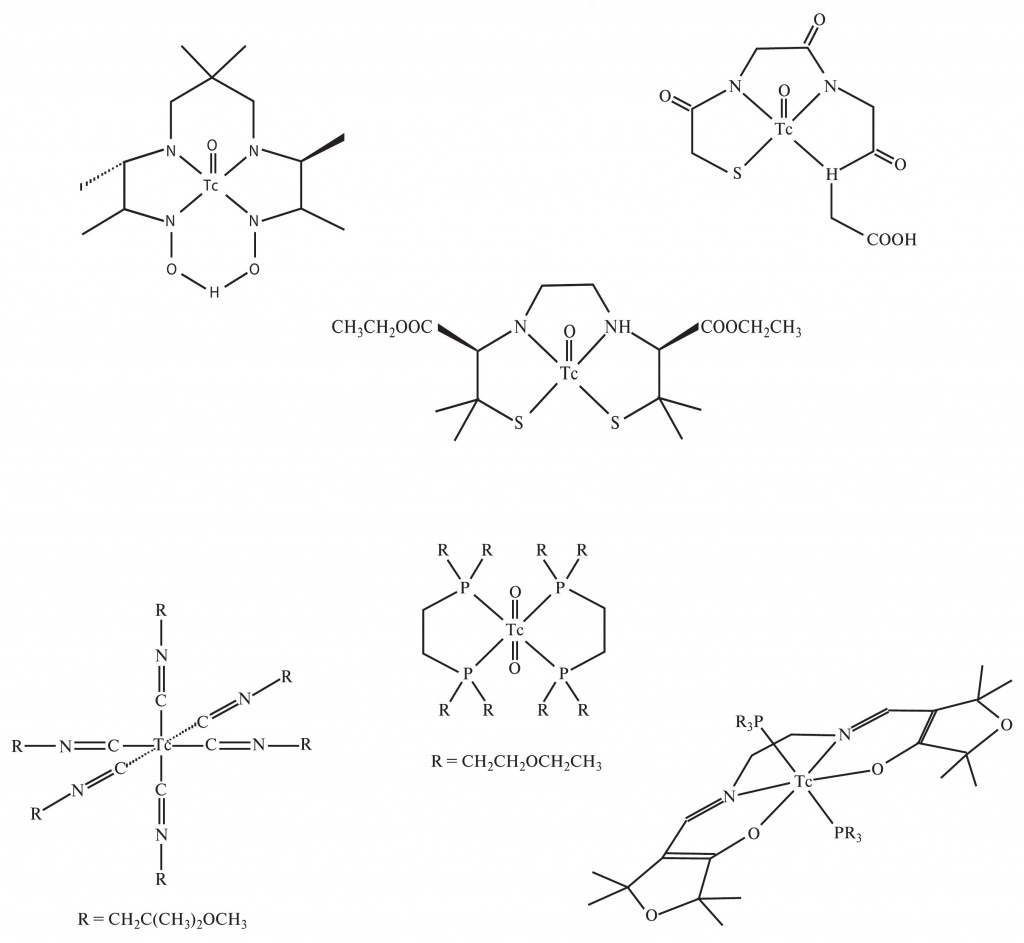 |
|
3. Структуры препаратов технеция |
У читателей, знакомых с понятием «горячие атомы», может возникнуть такой вопрос: если атом 99Мо в составе молибдат-аниона 99МоО42– превращается в результате β-распада в 99mТс, то как последний может оставаться в составе оксоаниона 99mТсО42–? Ведь при распаде возникает мощная «отдача»? В большинстве случаев это действительно так. Например, при α-распаде, когда из ядра с энергией в несколько МэВ вылетает тяжелая частица. Однако в данном случае из молибдат-аниона вылетает примерно в 7800 раз более легкий электрон с энергией 1,23 МэВ. Используя соотношения, известные из теории относительности, можно показать, что этот электрон имеет скорость vе = 2,87.108 м/с (т. е. 0,957 со), а его масса mе = 3,44mo. Теперь по табличным данным о скорости света (со) и массе покоя электрона (mo) можно рассчитать кинетическую энергию ядра: 15,2 эВ (1470 кДж/моль). Энергия возбуждения аниона ТсО42– меньше; она зависит от соотношения масс Тс и его окружения (4 атома кислорода) и равна 15,2(64/163) = 6,0 эВ (580 кДж/моль). Это сравнительно немного, и этой энергии не хватит для разрыва всех четырех связей Тс–О (для сравнения, энергия разрыва связи в оксиде молибдена МоО в газовой фазе равна 503 кДж/моль).
Эксперимент
Все оказалось предельно просто. Достаточно было позвонить в Межклиническое радионуклидное диагностическое отделение (далее МРДО) при Московской медицинской академии им. И.М.Сеченова, назвать свою фамилию и тип желаемого обследования. Даже направления не потребовали (мало кто захочет добровольно подвергнуться облучению – пусть и небольшому). Поскольку препарат готовят для конкретного пациента, запись ведется на строго определенное время.
К назначенному времени сотрудник МРДО Наиля Абдулхаликовна Мустафина готовит нужный раствор. В данном случае это был препарат «пирфотех», из названия которого следует, что в нем присутствуют пирофосфат и технеций. Препарат был приготовлен из бесцветного сухого лиофилизата. В нем содержится 1,8 SnCl2 и 16,2 мг Na4P2O7. Из генератора технеция элюируют 5–10 мл раствора, содержащего 99mТс с объемной активностью от 185 до 1480 МБк/мл (мегабеккерелей; 1 Бк соответствует одному распаду в секунду). Если активность слишком высока, элюат разбавляют стерильным изотоническим раствором NaCl. Далее раствор с технецием набирают в шприц, вводят во флакон с лиофилизатом и встряхивают до растворения. Получается готовая к применению бесцветная прозрачная жидкость с рН 5,1. Препарат, который приготовлен на основе лиофилизата, содержащегося в одном флаконе, может быть использован для исследования пяти пациентов. Как сообщал висевший на стене плакат, в диагностическом отделении, помимо скелета, можно исследовать щитовидную и паращитовидную железу, сердечную мышцу и работу желудочков сердца (вентрикулография), почки, головной мозг, мочевой пузырь, легкие, надпочечники. И для каждого исследования готовится свой препарат; помимо пирфотеха, это может быть пертехнетат, технетрил, пентатех, макротех и другие. Из некоторых названий сразу видна область применения. Например, тетрафосмин (MyoView) – для исследования миокарда, пульмоцис (МАА – макроагрегаты альбумина) – легких и т. д. Если человеку ввести внутривенно сначала раствор того же лиофилизата, о котором говорилось выше, а через полчаса – раствор пертехнетата, то при такой методике происходит мечение технецием эритроцитов. Мне ввели 500 МБк. Несмотря на устрашающую цифру (500 миллионов распадов в секунду!), нетрудно было тут же подсчитать, сколько технеция в граммах было в шприце. Времени же было достаточно: сцинтиграфию должны были провести, судя по инструкции, через три часа. Поскольку радиоактивный распад – реакция 1-го порядка, его скорость подчиняется уравнению W = kN, где W = 5·108 с–1, N – число атомов, а константа k легко определяется через период полураспада: k = ln2/t1/2 = 0,693/(6,04·3600) = 3,19·10–5 с–1. То есть, в моем организме оказалось N = W/k = 5·108/3,19·10–5 или 1,57·1013 атомов технеция-99m весом примерно 2,6 нг. Для нерадиоактивных веществ – ничтожно малое, невидимое глазом количество. И понятно, что находящийся в огромном избытке сильный восстановитель – двухвалентное олово немедленно восстанавливает атомы Тс(VII) до более низкой степени окисления, после чего они связываются в комплекс с пирофосфатом.
Пока препарат распределялся током крови по организму и оседал на костях скелета (на это требовалось некоторое время), было время подсчитать и количество технеция, и время его полного распада. Последнее легко сделать, поскольку период полураспада 99mТс – практически точно четверть суток. Значит, через сутки останется 1/24 = 1/16, через двое суток – 1/28 = 1/256 и т. д. Нетрудно подсчитать и когда в организме останется «последний атом»: 2n = 1,6.1013, где n – число периодов полураспада, откуда n = 44 (11 суток). Однако Наиля Абдулхаликовна сказала, что расчет неверен, поскольку я не учел биологический фактор вывода технеция из организма. Действительно, в «Инструкции по медицинскому применению препарата Пирфотех, 99mТс (информация для специалистов)» сказано, что после внутривенного введения пирфотех «выводится из крови и накапливается в скелете. Через 1 ч в скелете накапливается более 30% введенного количества. Через 3 ч после инъекции в крови содержится 10 – 15% препарата. Экскретируется из организма мочевыделительной системой. За 1 ч после введения выводится с мочой 30%, за 3 ч – 45% препарата».
Прошло нужное время, и меня уложили на столик томографа (рис. 4), который поехал в одну сторону, потом в другую, отсканировав меня от макушки до пяток. Заведующий отделением кандидат медицинских наук Сергей Платонович Паша рассказал потом, что при этом происходит. Испускаемые при изомерном переходе 99mТс > 99Тс гамма-кванты попадают на сцинтиллятор – монокристалл иодида натрия, активированного таллием. Там они вызывают вспышки света, которые регистрируются 96 фотоумножителями. Монокристаллы толщиной около 1 см и размером 60х40 см делают в Харьковском институте монокристаллов, а томограф американской фирмы «General Electric» собран в Хайфе. Сигнал с детекторов поступает для обработки на компьютер. Чтобы накапливающийся в мочевом пузыре технеций не давал «засветки», этот орган виртуально закрывают непрозрачным экраном, хорошо видным на снимке.
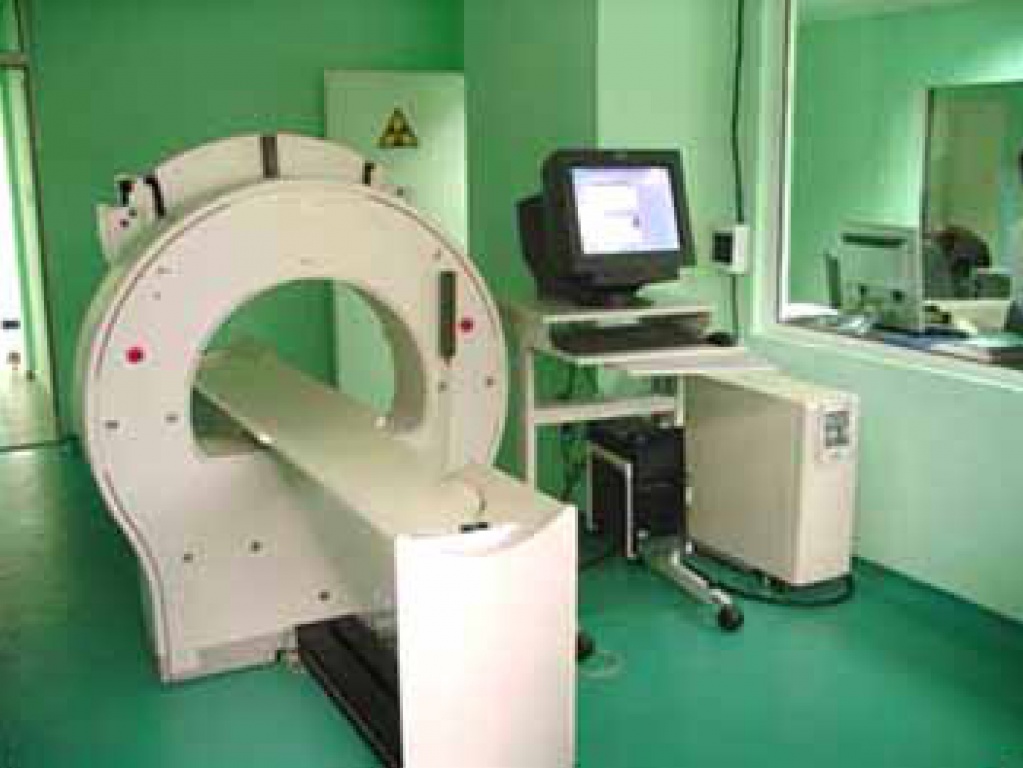 |
4. Томограф для сцинтиграфии |
Осталось привести выданное мне заключение – то, ради чего люди и приходят в диагностическое отделение. Из него видно, какого типа информацию может получить специалист в результате исследования. «На сцинтиграммах всего тела, выполненных в передней и задней прямых проекциях, отчетливо визуализируется включение пирофосфата в костные структуры. Накопление индикатора достаточной интенсивности, в парных костных образованиях симметричное. Распределение радиофармпрепарата соответствует возрастной норме. Зоны разреженной костной ткани и/или очаги патологической гиперфиксации индикатора не выявлены. Остаточная радиоактивность в почках и мочевыводящих путях соответствует времени исследования. Атипичная фиксация РФП в паренхиматозных органах и мягких тканях не отмечена. Заключение: признаки очагового поражения костей не выявлены. Врач А.И.Корнев». Как говорили древние, quod erat demonstrandum – что и требовалось доказать.
Что еще можно прочитать о технеции и его применении в медицине:
Л.Л.Зайцева, А.В.Величко, И.В.Виноградов. Соединения технеция и области их применения. М., 1984.
P.T.Buckley, D.L.Dugan, J.T.Elliston, R.H.Filby, J.J.Lessmann, Alena Paulenova. Radioisotopes in medicine: operating a technetium-99m generator and determining its efficiency. J. Chem. Education, 2006, vol. 83, No. 4, pp. 625 – 626.
S.S.Jurisson, J.D.Lydon. Potential technetium small molecule radiopharmaceuticals; Shuang Liu, D.S. Edwards. 99mTc-Labeled small peptides as diagnostic radiopharmaceuticals. Chem. Reviews, 1999, vol. 99, No. 9 (этот номер целиком посвящен медицинской химии, в том числе и радиоактивным фармацевтическим препаратам).
J.R.Dilworth, S.J.Parrott. The biomedical chemistry of technetium and rhenium. Chemical Society Reviews, 1998, vol. 27, pp. 43 – 55. Эта статья доступна в Интернете: http://www.rsc.org/ej/CS/1998/a827043z.pdf
