
Подписаться
Подписаться
Вылечит ли бацилла сахарный диабет?
 |
|
Художник С. Дергачёв |
Когда ученые сообщают, что почти нашли новое лекарство от диабета, очень хочется им верить, особенно если данные получены в престижном исследовательском центре и опубликованы в авторитетных международных журналах. Увы, все это не гарантирует от разочарования.
Двадцать лет по торной дороге
Сахарный диабет первого типа — аутоиммунное заболевание, при котором разрушаются бета-клетки поджелудочной железы, синтезирующие инсулин. Из-за нехватки этого гормона глюкоза не поступает в клетки, а ее уровень в плазме крови повышается. Лечат болезнь инъекциями инсулина, но всех проблем этот метод не решает, поскольку поджелудочная железа продолжает разрушаться. Исследователи пробуют разные методы восстановления бета-клеток (см. «Химию и жизнь», 2018, 12).
Диабет развивается из-за нарушений в работе иммунной системы. Она содержит цитотоксические Т-лимфоциты, они же Т-киллеры, которые должны уничтожать чужеродные клетки. Но иногда случаются сбои. При диабете первого типа лимфоциты-киллеры становятся аутоиммунными и избирательно атакуют бета-клетки поджелудочной железы. В подобных случаях на помощь должны прийти регуляторные Т-лимфоциты, задача которых – уничтожать аутоиммунные клетки. Однако при аутоиммунных заболеваниях регуляторных клеток либо мало, либо они не работают, но результат один: со своей задачей они не справляются, и аутоиммунные Т-клетки продолжают бесчинствовать. Есть еще одно средство — фактор некроза опухоли, внеклеточный белок, который синтезируют другие клетки иммунной системы — макрофаги. Он убивает любые аутоиммунные лимфоциты, а здоровые не трогает. Это давно и хорошо известно, однако использовать белок как лекарство нельзя — он токсичен для людей.
Иммунологи Массачусетской больницы широкого профиля и Гарвардской медицинской школы под руководством доцента Дениз Фаустман исследуют диабет первого типа 20 лет. Они работали с традиционным модельным объектом для изучения диабета — мышами линии NOD. У этих животных спонтанно возникает аутоиммунное заболевание, сходное с диабетом человека. В 2001 году доктор Фаустман сообщила о том, что стимулировала у своих мышей усиленный синтез фактора некроза опухоли, отчего у больных животных восстановились островки бета-клеток в поджелудочной железе. Вот бы и людям так! Но, увы, просто дать пациенту дозу белка нельзя. Нужно, чтобы организм сам увеличил его синтез, и ученые уже полсотни лет, не меньше, знают, как этого добиться. Макрофаги выделяют фактор некроза опухоли в ответ на бактериальную инфекцию, и, когда их нужно стимулировать, людям или животным вводят противотуберкулезную вакцину БЦЖ (бациллу Кальмета — Герена) — ослабленный, но живой возбудитель туберкулеза крупного рогатого скота Mycobacterium bovis. Эту вакцину используют почти сто лет, привили более 3 миллиардов человек, и у исследователей были время и возможность заметить, что она активирует неспецифический иммунный ответ, то есть реакцию организма на любую инфекцию.
Именно этим испытанным средством воспользовались гарвардские иммунологи. В 2010 году они начали первый этап клинических исследований, который занял 8 лет и прерывался из-за проблем с финансированием. Испытуемых случайным образом разделили на две группы, которым дважды с интервалом в четыре недели внутрикожно вводили БЦЖ или плацебо. В течение 8 лет им регулярно делали анализы крови и сравнивали показатели с результатами здоровых людей и больных, которым не делали никаких инъекций.
Инъекции вакцины привели к двум существенным результатам. Прежде всего они нормализовали состояние иммунной системы пациентов. В течение первых восьми недель у них погибли почти все аутоимунные Т-клетки: пик смертей пришелся на пятую неделю эксперимента (после второй инъекции). В то же время «исцелились» испорченные регуляторные Т-лимфоциты. Они не работали из-за того, что у них были метилированы несколько ключевых генов. Вакцинация вызвала деметилирование, гены заработали нормально, и регуляторные клетки смогли вернуться к выполнению своих обязанностей.
Кроме того, вакцина повлияла на глюкозный метаболизм лимфоцитов. У больных диабетом первого типа глюкоза в клетки практически не поступает. Чтобы получать необходимую энергию и синтезировать АТФ, они вынуждены окислять не глюкозу, а жирные кислоты. После инъекций глюкоза потекла из плазмы крови в клетки, которые ее расходовали для синтеза АТФ, нуклеотидов и некоторых аминокислот. В результате концентрация глюкозы в крови снизилась. Эти изменения исследователи выявили, сравнив последовательности ДНК, мРНК и метаболиты в клетках испытуемых и участников групп сравнения.
 |
|
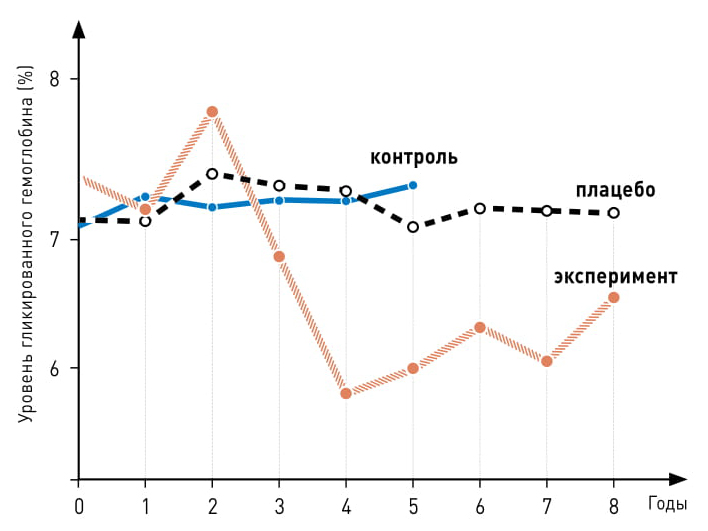
После двух инъекций БЦЖ у больных диабетом первого типа (СД1) меняется уровень гликированного гемоглобина |
В качестве показателя уровня глюкозы в крови ученые использовали долю гликированного гемоглобина. Гемоглобин находится в эритроцитах, и какая-то его часть необратимо связана с молекулами глюкозы. Чем выше была средняя концентрация сахара в крови за последние три месяца, тем больше доля гликированного гемоглобина. В начале исследования этот показатель составлял в среднем 7,36%, что близко к верхней допустимой границе для больных диабетом первого типа. За 5 лет этот уровень снизился у вакцинированных пациентов до 6,18%, потом, правда, подрос до 6,65%, но это все равно лучше, чем было. У группы плацебо и участников групп сравнения показатели не изменились (см. график на рис.)
Дениз Фаустман и ее коллеги очень гордятся полученным результатом. Они утверждают, что БЦЖ снижает уровень сахара в крови, влияя на экспрессию генов, регулирующих поступление глюкозы в клетки и ее утилизацию. При этом поступление глюкозы в клетки зависит от ее концентрации в крови: если концентрация мала, лимфоциты прекращают поглощать сахар, поэтому гипогликемия больному не грозит. Инсулиновые инъекции снижают уровень глюкозы, невзирая на изменения ее концентрации, и риска гипогликемии не избежать.
К сожалению, этого замечательного результата придется подождать: уровень гликированного гемоглобина почему-то снижается лишь спустя 3–4 года после введения БЦЖ. У мышей, больных диабетом, уровень глюкозы в крови тоже снижался не сразу после вакцинации, а через шесть недель. Учитывая, что мышь в среднем живет 2,5 года, этот срок сопоставим с 3,5 годами человеческой жизни. Возможно, для сокращения сроков нужно увеличить дозу БЦЖ и делать больше инъекций.
А теперь о грустном. БЦЖ не восстановила бета-клетки поджелудочной железы. Несколько недель после инъекций синтез инсулина увеличивался, но быстро вернулся к прежнему уровню. Результат, полученный на мышах, не удалось повторить на людях. Возможно, причина в том, что экспериментальные грызуны были молоды, а люди ко времени вакцинации уже имели за плечами по 15–20 лет болезни. Не исключено, что вакцина сможет вылечить детей (диабет первого типа проявляется в раннем возрасте); так ли это, покажут педиатрические испытания, если до них дойдет дело.
Таким образом, эффект вакцинации свелся к снижению уровня глюкозы в крови, не зависящему от синтеза инсулина, что может, по мнению Дениз Фаустман, изменить стандарты лечения диабета первого типа. Исследовательница подчеркивает, что для лечебного эффекта необходима двойная вакцинация с интервалом в несколько недель, однократная не поможет. Все нерешенные вопросы ученые планируют выяснить на втором этапе клинических испытаний, которые должны завершиться в 2023 году. Пока для этой работы не хватает денег. Фаустман не удалось получить грант, ее исследования финансируют частные фонды и добровольные жертвователи. Из 20 миллионов долларов, необходимых для работы, удалось собрать примерно половину.
Три плюс шесть
Трудности не обескуражили исследовательницу. В прошлом году она опубликовала результаты в журнале «npj Vaccines», партнере «Nature», затем появилась статья в «Trends in Endocrinology & Metabolism», входящем в издательскую группу «Cell». А в июне прошлого года доктор Фаустман представляла свои результаты на научной сессии Американской диабетической ассоциации. Накануне конференции она встретилась с журналистами, и в день открытия сессии ведущие популярные издания пестрели заголовками типа: «Нашла ли д-р Фаустман лекарство от диабета первого типа?»
По правилам на конференции можно докладывать только новейшие результаты, которые еще не были опубликованы, и уж тем более не разрекламированы в СМИ. Исследовательница эти правила нарушила, чем обидела и Американскую диабетическую ассоциацию, и Фонд исследования ювенильного диабета, который в свое время отказал Дениз Фаустман в финансировании. То ли неудовольствие, то ли научная добросовестность побудила экспертов обеих организаций выступить с совместным заявлением (небывалый случай!), в котором они обратили внимание общественности на некоторые методические подробности данного исследования. Сама доктор Фаустман эти детали не то чтобы скрывала, а просто не афишировала, и рецензенты престижных научных журналов почему-то не придали им значения.
По мнению экспертов, полученные результаты, хотя и предлагают наводящие на размышление вопросы, не дают на них однозначных ответов, а клинических данных недостаточно, чтобы давать какие-то рекомендации по лечению диабета первого типа.
Начнем с числа испытуемых. Гарвардские иммунологи пишут, что их было 282, однако большую часть составили участники группы сравнения. Вакцинированных пациентов поначалу было всего трое, это за ними наблюдали 8 лет. Позже к исследованию присоединились еще шестеро и участвовали в пятилетних исследованиях. Итого девять вакцинированных и еще трое в группе плацебо. Эти подробности упомянуты в статьях либо вскользь мелким шрифтом, либо в дополнении, которое доступно только в электронном виде. Эксперты утверждают, что такого числа испытуемых недостаточно, тем более что в первой тройке вакцинированных БЦЖ подействовала только на двоих.
Также мимоходом авторы работы сообщают, что в ходе исследования все больные продолжали принимать инсулин. О подробностях терапии в разных группах ученые не пишут. Поэтому нет оснований утверждать, что вакцинация БЦЖ меняет стандарты лечения диабета первого типа. Вы спросите, как в таком случае исследователи различали инсулин, синтезируемый в поджелудочной железе и получаемый извне? По уровню С-пептида. Он образуется в бета-клетках при расщеплении проинсулина и вместе с гормоном выделяется в кровоток. Сколько синтезировалось инсулина, столько и С-пептида образовалось. До 20-й недели его уровень потихоньку рос и стал примерно вдвое больше, чем в группе сравнения, а потом пошел на убыль.
Что касается гликированного гемоглобина, его концентрация снизилась весьма умеренно. Критики отмечают, что этот эффект может быть не связан с вакцинацией и нет гарантии, что он воспроизведется у миллионов больных. Кроме того, концентрация гликированного гемоглобина у больных диабетом имеет тенденцию со временем снижаться сама собою, особенно после того, как пациенты выходят из подросткового и юношеского возраста. Дениз Фаустман это явно не учитывает. А еще она не может повторить результаты, полученные на мышах в 2001 году (одни сотрудники лаборатории говорят, что островковые клетки у мышей все-таки восстанавливаются, другие утверждают, что нет).
Обе организации заявляют, что в настоящее время не финансируют работу доктора Фаустман, но будут следить за ее развитием. Это заявление вызвало множество откликов заинтересованных людей. Кто-то называет исследовательницу мошенницей, внушающей ложные надежды. Люди, пожертвовавшие деньги на исследования, требуют их вернуть и недоумевают, на что исследователи потратили 20 лет. Другие продолжают надеяться.
Сама Фаустман отвечает, что ее данные статистически верны: на то и существует статистика, чтобы оценивать достоверность результатов, полученных на малых выборках. У пациентов, которым сделали две инъекции БЦЖ, в течение более чем 5 лет наблюдалось статистически значимое изменение гликированного гемоглобина без каких-либо серьезных осложнений или тяжелых гипогликемических событий по сравнению с плацебо. Эти наблюдения дают основания перейти ко второму этапу исследований, во время которого иммунологи рассчитывают получить больше информации об эффектах БЦЖ. В этой фазе клинических испытаний участвуют 150 человек, в том числе 120 вакцинированных. Наблюдение за ними продлится 5 лет, один год уже прошел. Кроме того, ученые заняты разработкой биомаркеров, которые позволят быстро определить изменение метаболизма глюкозы, и сравнением эффективности разных штаммов БЦЖ. Они также планируют педиатрические исследования и интересуются влиянием вакцины на другие аутоиммунные заболевания. В общем, планов много, были бы деньги и разрешение контролирующих органов. Дениз Фаустман рассчитывает получить и то и другое.
Не только БЦЖ, не только диабет
Поскольку БЦЖ стимулирует иммунный ответ на любую инфекцию, она полезна при многих заболеваниях. Еще в 1930-х годах медики заметили, что вакцина заметно снижает детскую смертность, и этот эффект нельзя объяснить одной профилактикой туберкулеза. А с 1970-х годов ее используют для лечения меланомы, рака мочевого пузыря, некоторых заболеваний, вызванных микроорганизмами рода Mycobacterium, в том числе проказы. Она сокращает риск развития атопии (предрасположенности к аллергическим реакциям). Все эти данные получены в ходе клинических исследований и популяционных наблюдений.
А диабет первого типа инъекциями БЦЖ пытались лечить давно, но без особого успеха. При ранней иммунизации у мышей NOD они предотвращают развитие диабета. У людей, привитых в детстве, вакцина не предупреждает болезнь, но, возможно, отсрочивает ее начало. В исследовании, проведенном в 1994 году в Израиле, у 11 из 17 пациентов, недавно заболевших диабетом первого типа, однократная инъекция БЦЖ вызвала ремиссию. В контрольной группе таких счастливчиков было только двое из 29. С другой стороны, сколько лет уже новорожденным делают прививку БЦЖ, а заболеваемость диабетом растет. В общем, вакцина если и влияет на диабет, то очень слабо. Возможно, Дениз Фаустман права и вакцинировать надо дважды.
Ослабленная бацилла коровьего туберкулеза — не единственная инфекция, которая взбадривает иммунную систему. Это тоже давно известно, и примером могут служить результаты, полученные в лаборатории Фаустман. У одного из участников группы плацебо аутоиммунные Т-лимфоциты погибли, регуляторные восстановили функциональность, а уровень гликированного гемоглобина снизился, как у вакцинированных пациентов. Оказалось, что этот человек заражен вирусом Эпштейна — Барр, который также стимулирует экспрессию фактора некроза опухоли. Но вирусная инфекция, конечно, не метод лечения, надо подобрать средство помягче.
Это сейчас медики ищут вакцины, способные предотвратить диабет, а еще лет 30 назад считали, что прививки могут повышать риск развития диабета первого типа. Проверяя эту гипотезу, сотрудники Каролинского института (Швеция) в 1991 году собрали сведения о 339 детях, недавно заболевших диабетом первого типа, и 528 здоровых детях в возрасте от младенческого возраста до 14 лет. Оказалось, что вакцинации против туберкулеза, оспы, столбняка, коклюша, краснухи и эпидемического паротита не повлияли на риск развития диабета у юных шведов, зато вакцина от кори снизила вероятность заболевания.
Выводы о связи между иммунизацией и диабетом первого типа пока сделать трудно. Нужно больше информации. Возможно, медики научатся предотвращать болезнь, используя уже существующие вакцины, или специально создадут новые. А нам остается ждать и надеяться на их удачу и научную добросовестность.
Эта статья доступна в печатном номере "Химии и жизни" (№ 9/2019) на с. 27 — 29.