Бионический фермент - уже не фантастика
Возможно, скоро появится новый способ получения лекарств, пестицидов и других веществ, необходимых нам в повседневной жизни. Ученым из Национальной лаборатории Беркли, работающим под руководством Джона Хартвига, удалось впрячь в одну телегу «коня и трепетную лань». Они получили катализатор для ускорения принципиально новых химических реакций («Nature», 2016; doi: 10.1038/nature17968).
Исследователи получили металлопротеин, заместив железо, входящее в состав белка мышечной ткани (миоглобина), иридием — благородным металлом, который, как известно, в биомолекулах не встречается. Оказалось, что иридийсодержащий миоглобин может ускорять новый тип химической реакции — конверсию связи С-Н в связь С-С. Таким образом, бионический фермент катализирует реакцию, которую не могут катализировать ни природные, ни модифицированные ферменты.
По словам Хартвига, еще никому до сих пор не удавалось соединить два разных типа катализатора в одну систему. Таким же способом можно будет синтезировать бионические катализаторы для любой области химии, в которой необходимы быстрые и селективные каталитические процессы.
Ферменты, то есть биологические катализаторы белкового строения, ускоряют реакции в живых организмах. Они имеют много преимуществ перед синтетическими катализаторами: синтезируются сами, очень селективны, работают при температуре, близкой к комнатной, и нормальном атмосферном давлении, в водной среде и при значениях рН, близких к нейтральным. Современные методы молекулярной биологии позволяют модифицировать ферменты, вырабатываемые живыми организмами, увеличивать их активность, селективность и долговечность.
|
|
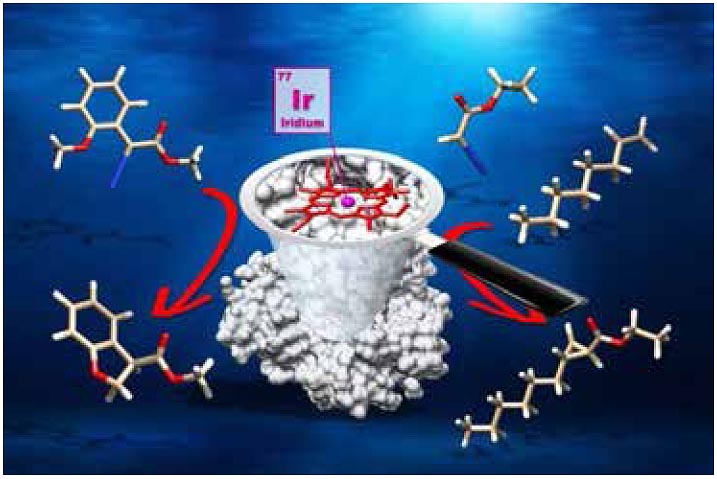
Схематичное представление искусственного металлопротеина. Порфириновый центр сложного белка природного происхождения (пептидная часть белка — белая) содержит не обычное для гемового центра железо, а иридий (в центре). Фермент ускоряет присоединение связи С-Н к двойной связи С=С и образование новой связи С-С |
Несмотря на столь очевидные преимущества ферментов в сравнении с синтетическими катализаторами, есть у них и недостаток — круг реакций, которые ферменты катализируют, все же узок. Ферменты незаменимы при получении молекул, которые нужны для жизни и производятся живыми системами, но практически непригодны для получения синтетических органических веществ, таких как полимеры или лекарства.
Дело в том, что металлы, входящие в состав активных центров ферментов — железо, медь или хром (чаще всего они управляют работой окислительно-восстановительных процессов), не в состоянии конкурировать со «стандартами» современного гомогенного металлокомплексного катализа — платиной, иридием, рутением или палладием. Именно эти благородные элементы могут ускорять ключевой для современной синтетической химии процесс — образование связи С-С.
Суть идеи в том, чтобы заменить железо в миоглобине на иридий и объединить синтетические возможности благородных металлов и способность ферментов работать в мягких условиях. Как показали исследования, идея себя оправдала, и теперь уже вполне можно говорить о новом типе катализаторов — бионических ферментах, содержащих в активном центре металлы платиновой триады.
