Российские «короны» и другие ценности
Начало: Ловушки для атомов
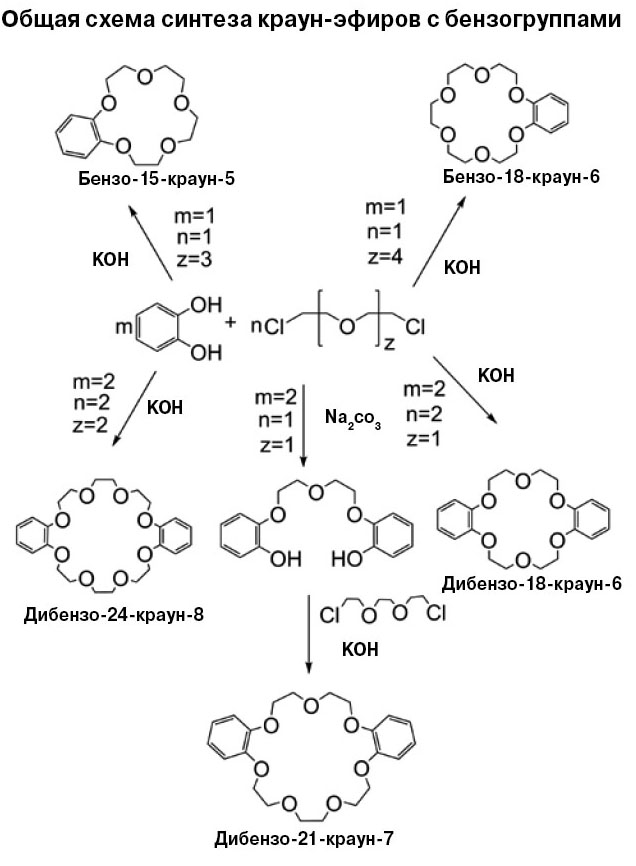
Первыми соединениями, полученными с помощью установки в ИРЕА, были дибензо-21-краун-7 и дибензо-18-краун-6 («Химическая технология», 2013, 7, 412—419; «Наукоемкие технологии», 2013, 3, 5—10). Основой синтеза стали химические реакции, предложенные Чарльзом Педерсеном. Но перед тем как отправить реагенты в реактор, процесс доработали, подобрали нужные растворители, устранили побочные реакции и лишь затем запустили производство. Сейчас на установке получают больше десяти разных краун-эфиров.
|
|
| Дибензо-21-краун-7 |
В лаборатории В.Н.Глушко изучают краун-эфиры, в структуре которых на месте одного из кислородов находится азот («Journal of Structural Chemistry», 2015, 56, 1, 142—147). Это усиливает ион-дипольное взаимодействие, связи становятся более прочными, решетка сжимается, ее объем уменьшается, а значит, внутри могут оказаться более юркие атомы: никель, медь, железо, платина.
|
| Несколько слов о номенклатуре краун-эфиров. Чтобы дать молекуле название, сначала определяем тип и число замещенных групп в полиэфирном кольце. Например, в данном случае два бензольных кольца — «дибензо». Затем пишем число атомов в кольце (21) — это число характеризует и размер полости. Затем «краун» и число атомов кислорода, то есть эфирных звеньев в кольце (7): дибензо-21-краун-7. |
Краун-эфиры применяют также для фотометрического и флуоресцентного анализов, фотоуправляемой экстракции. Так, избирательность краунов очень пригодилась для изготовления различных сенсоров.
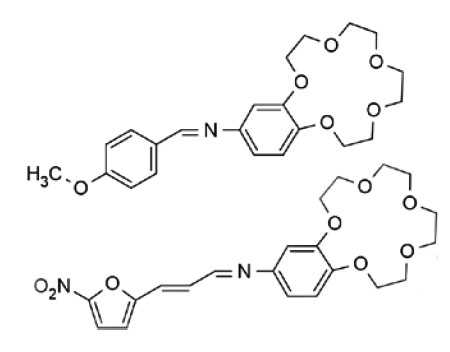
Сигнальная часть сенсора — флуорохром — сильно поляризуется, когда в растворе к нему приближаются катионы или анионы металлов, и как бы направляет их к рецептору, например краун-эфиру. В этот момент можно зафиксировать люминесценцию и по ее интенсивности узнать состав и количество определяемого вещества в пробе, в частности катионов Сu2+, Zn2+, Fe 3+, Co 3+, Ni 3+ .
|
| Хромогенные сенсоры на катионы Сu2+ — азометиновые производные на основе 4-аминобензо-15-крауна-5. В лаборатории получили разные их производные по схеме, показанной ниже |
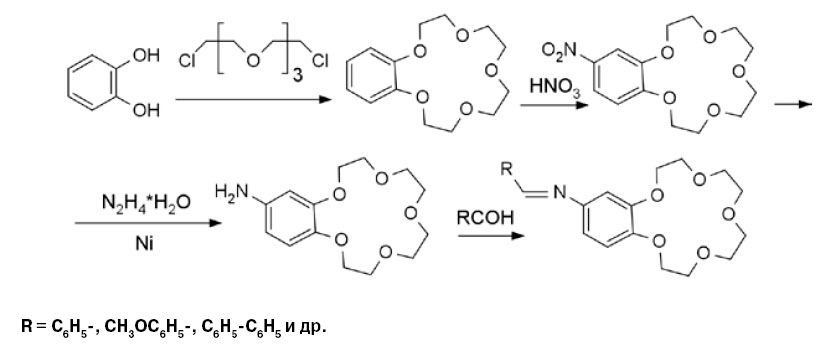
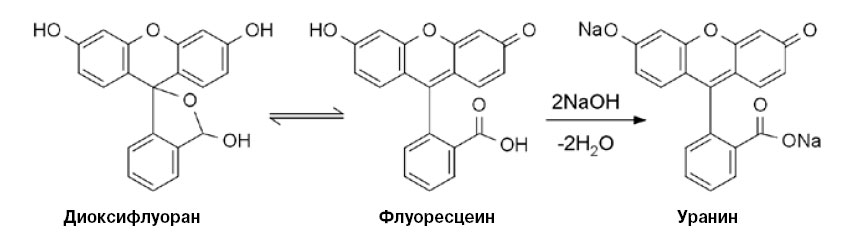
В качестве флуорохрома можно использовать флуоресцеин. Его бесцветная лактонная форма — диоксифлуоран в результате таутомерного превращения быстро переходит в желтую хиноидную форму. Желтовато-красные щелочные растворы флуоресцеина светятся зеленым в ультрафиолетовых лучах. Флуоресценция заметна и при сильном разбавлении водой, поэтому краситель используют с целью профилактики для определения течей в промышленных канализациях — или ради развлечения, например, в День святого Патрика именно флуоресцеином окрашивают реку Чикаго в зеленый цвет. Ярко-желтую динатриевую соль флуоресцеина — уранин применяют для окрашивания морских опознавательных знаков.
|
| Флуоресцеин и его «родственники» — диоксифлуоран и уранин. Из-за яркого зеленого свечения флуоресцеин находит самые разнообразные применения. Работает он и в паре с краун-эфирами |
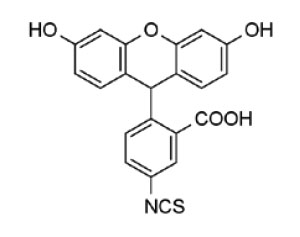
А вот изотиоцианатные аналоги флуоресцеина могут «покрасить» даже антитела. При этом флуорохром ковалентно присоединяется к биомолекулам через NCS-группу флуоресцеин-изотиоцианата.
|
| В лаборатории перспективных органических реактивов впервые создали условия для эффективной очистки флуоресцеин-5-изотиоцианата |
Антитела с флуоресцентной меткой необходимы для быстрой диагностики инфекций. Иммунофлуоресцентную реакцию между антителом, меченным флуорохромом, и белками-антигенами на поверхности бактериальной клетки или вируса можно наблюдать в лучах лазера. По интенсивности свечения флуорохрома определяют концентрацию патогенных микроорганизмов, субпопуляционный состав, размер клеток в пробе за 10—15 минут, а иногда и за секунды («Российский химический журнал», 2014, 58, 1, 40—45).
