Гидразин космический
История с предысторией
В том, что гидразин был открыт в самом конце XIX века, сомневаться не приходится. Однако, отыскав статью об этом веществе в Краткой химической энциклопедии, вы так и не узнаете, кто же его открыл. А в специальной литературе фигурируют имена как минимум двух первооткрывателей. Обратимся к источникам авторитетным и доступным.
В менделеевских «Основах химии», равно как и в «Истории химии» Микеле Джуа, первооткрывателем гидразина назван Теодор Курциус (1857—1928) — известный в свое время химик, профессор в Киле и Гейдельберге, первым получивший еще несколько веществ, главным образом азотсодержащих.
Однако во французских книгах по истории химии утверждается, что чистый безводный гидразин был получен лишь через семь лет после опытов Курциуса, в 1894 году, французским химиком Лобре де Брином. Курциус же получил лишь сульфат гидразина — соль состава N2H4-H2SO4.
Как бы там ни было, справедливости ради нужно отметить, что открытию неорганического вещества гидразина предшествовали работы трех очень известных химиков-органиков. Еще в 1845 году Николай Николаевич Зинин, тогда еще молодой профессор Казанского университета, восстановив азобензол сернистым натрием, получил бесцветные пластинки гидразобензола — первого вещества, содержащего группу — NH — NH—. (Формула этого соединения C6H5NHNHC6H5, его можно считать первым известным нам производным гидразина.) Через тридцать лет немецкие химики Эмиль и Отто Фишеры (первый стал Нобелевским лауреатом) выделили фенилгидразин C6H5NHNH2. По сути дела, они смогли заменить атомом водорода одну из фенильных групп молекулы гидразобензола. Когда то же самое удалось сделать и со второй фенильной группой, гидразин предстал перед химиками в относительно чистом виде...
Как он есть
Не слишком привлекательно выглядело новое вещество. Бесцветная довольно вязкая жидкость, дымящаяся на воздухе, с запахом нашатырного спирта, не очень стойкая к окислителям (склонная к самовоспламенению) и гигроскопичная. Но были у гидразина свойства, заинтересовавшие химиков. Например, он оказался восстановителем, причем очень активным. Окислы многих металлов — железа, хрома, меди — при контакте с ним восстанавливались столь бурно, что избыток гидразина воспламенялся и горел синим (точнее все-таки фиолетовым) пламенем.
Позже выяснили, что под действием этих окислов происходит каталитическое разложение гидразина на газообразные азот и аммиак. Таким образом, он оказался пригоден в качестве ракетного топлива. Но с этой точки зрения гидразином заинтересовались спустя много лет. Пока же его изучали как достаточно своеобразный химический феномен.
Отметили, в частности, что в полярных жидкостях (вода, амины, спирты) гидразин растворяется очень хорошо, в неполярных же, и прежде всего в углеводородах, он растворяться не желает. Раствор гидразина в воде, как выяснилось, имеет состав N2H4-H2O, причем по физическим свойствам больше походит на воду безводный гидразин, нежели «водный». Сравним плотности, температуры замерзания и кипения этих трех веществ:
вода — 1,00 г/см3, 0° и 100°С,
гидразин — 1,01 г'см3, 2°С и 11 3,5°С,
гидразингидрат — 1,03 г/см3, —51,7°С и 119,5°С.
Обратим внимание на значительно более низкую температуру замерзания гидразингидрата. Именно это обстоятельство позволило использовать в качестве ракетного топлива гидразингидрат в тех случаях, когда сам гидразин замерзает.
Тепла при горении гидразина выделяется сравнительно мало—намного меньше, чем при горении углеводородов. Гидразингидрат в этом смысле еще хуже. Но оба они хорошо горят при малых затратах окислителя (последним могут быть воздух и кислород, перекись водорода, азотная кислота и фтор; кроме того, как мы уже знаем, гидразин может создавать реактивную тягу и без помощи реакции окисления, разлагаясь на катализаторах). Это обстоятельство, а также большое количество образующихся при горении газов сделали гидразин и его производные незаменимыми веществами ракетных полигонов.
Макро и микро
Двигателем второй ступени ракет «Космос», посредством которых в 1962— 1967 гг. на космические орбиты выведено около 200 искусственных спутников Земли, был жидкостной реактивный двигатель РД-119. Горючим для него служило вещество, обозначаемое в справочниках четырьмя буквами: НДМГ. Расшифровываются они так: несимметричный диметилгидразин. Еще одно важное для ракетной техники производное гидразина! Его формула: (CH3)2NNH2.
В отличие от безводного гидразина и гидразингидрата это вещество легко, в любых соотношениях, смешивается не только с водой, но и с нефтепродуктами. НДМГ входит в состав многих жидких ракетных топлив. Известное американское горючее для ЖРД «Аэрозин-50» это смесь гидразина и НДМГ.
НДМГ от гидразина отличается не сильно: то же агрегатное состояние, близкие химические и физические свойства, тот же малоприятный запах.
Одна существенная частность. Несимметричный диметилгидразин — хороший растворитель. Поэтому в нем набухают, утрачивая прочность и плотность, большинство известных прокладочных материалов. Исключение составляют лишь некоторые специальные резины, полиэтилен и, конечно, «пластмассовая платина» — фторопласт-4.
Пределы взрывоопасных концентраций для смесей НДМГ с воздухом чрезвычайно широки: от 2 до 99% НДМГ по объему. Уже поэтому лучше не допускать его контакта с воздухом. Но есть и другие причины. Во-первых, он окисляется кислородом; во-вторых, взаимодействует с двуокисью углерода, содержащейся в воздухе (при этом образуются твердые соли); в-третьих, как и гидразин, НДМГ поглощает из воздуха влагу. Все три процесса приводят к порче достаточно дорогого НДМГ. Потому эту непростую жидкость рекомендуют хранить под азотной «подушкой».
Выше рассказано о наиболее известных примерах использования гидразина и его производных в ракетной технике. Однако это был, если хотите, итог, высшая точка взлета. А предшествовали ей события менее знаменательные, не претендующие на долгую и благодарную память. Однако умолчать о них было бы неверно.
Многим читателям «Химии и жизни», очевидно, знакомо имя немецкого инженера и изобретателя Хельмута Вальтера. До начала второй мировой войны он был техническим руководителем небольшой приборостроительной фирмы, а к концу войны стал одним из самых почитаемых (и глубоко засекреченных) деятелей науки и техники в фашистской Германии. Как и Вернер фон Браун, он разрабатывал «оружие возмездия», на которое так рассчитывали гитлеровцы и которое им почти ничего не дало.
Вся карьера Вальтера связана с концентрированными растворами перекиси водорода. Их он использовал и в двигателях для подводной лодки новой конструкции (о чем рассказано в статье «Совершенно секретно: вода плюс атом кислорода» — «Химия и жизнь», 1972, № 1), и в реактивном двигателе собственной конструкции. Восьмидесяти процентная перекись водорода работала в этом двигателе как окислитель, горючим же для него служила смесь почти равных количеств метилового спирта и гидразингидрата. Гидразингидрат в составе топлива обеспечивал его легкое и безотказное самовоспламенение.
Двигатели Вальтера устанавливали на истребителях Мессершмитта «Ме-1 63» и на пилотируемом самолете-снаряде «Наттер». Последний предназначался для борьбы с бомбардировочной авиацией. Примитивная деревянная конструкция самолета несла мощный заряд из 24 твердотопливных реактивных снарядов. После залпа летчик и дорогостоящий двигатель спасались на парашютах, а «Наттер» самоуничтожался в воздухе.
Дальше испытаний (сентябрь 1944 г.) затея с «Наттером» не пошла. Она не повлияла на исход войны, как, впрочем, и другие начинания Хельмута Вальтера. Однако работы по использованию гидразина и его производных в качестве реактивного топлива были продолжены в разных странах. В частности, в США вскоре после войны построены ракеты «Бомарк», «Авангард», «Тор-Эйбл», «Найк-Аякс», работающие на смеси, несимметричного диметилгидразина и керосина. Позже НДМГ вошел в состав топлива двигателей второй ступени ракет «Тор-Дельта», «Торад-Дельта», «Тор-Аджена», «Торад-Аджена». Он же входил в состав горючего первой и второй ступеней мощных ракет-носителей «Титан-М», «Титан-Ill». А в реактивном двигателе французского истребителя- бомбардировщика «Мираж-111» НДМГ используют как активизирующую добавку к традиционному топливу.
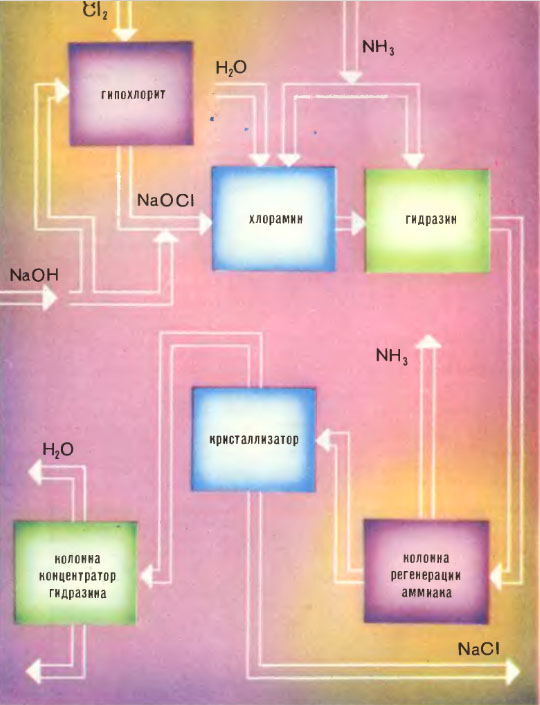 |
| Для получения гидразина в промышленных масштабах сейчас используют в основном два способа — окисление мочевины гипохлоритом натрия в щелочной среде и процесс взаимодействия аммиака с хлором в водном растворе каустической соды, разработанный еще в 1907 году известным химиком Фридрихом Рашигом. Схема этого процесса и показана на рисунке. Слегка видоизмененным этот же способ используют и для получения важнейшего из производных гидразина — несимметричного диметилгидразина |
Есть сведения, что гидразин и его производные будут работать и при полетах «космического челнока» — транспортного космического корабля многократного действия «Спейс шаттл», проект которого разработан в США.
Современной космической технике нужны не только гигантские двигатели ракет первой и второй ступени. В последнее время все больше внимания уделяют разработке микрореактивных двигателей, с помощью которых корабли и спутники перемещаются в открытом космосе в условиях невесомости — меняют орбиты, маневрируют. В этих микродвигателях гидразину тоже отводят важную роль.
В условиях орбитального полета одним из самых главных требований к ракетному топливу становятся простота и надежность его воспламенения (или начала реакции самопроизвольного разложения с выделением газообразных продуктов). С этой точки зрения гидразин и его производные не имеют равных. Они воспламеняются очень легко, а разложение гидразина на азот и аммиак возможно как под действием нагрева, так и под влиянием катализаторов. В итоге микродвигатели с гидразином и его производными изготавливают в нескольких странах. Известно, например, что гидразиновые микродвигатели будут работать уже в начале 80-х годов в системах ориентации и коррекции орбиты нового европейского спутника связи «ECS». Сообщалось также, что бре- менская фирма «Эрно» выпустила двадцать гидразиновых микродвигателей с тягой от 0,5 до 2,0 Н (50—200 гс) для спутника «OTS», запущенного Европейским космическим агентством в прошлом году.
Но не только в космосе, не только для космической техники нужен нам гидразин. Сегодня химии гидразина посвящено много исследований и книг. Производных его получены сотни тысяч, и некоторые из них оказались практически значимыми.
В терапевтической практике используют многие биологически активные вещества — производные гидразина. Известна, в частности, группа лекарств от туберкулеза, в которых действующим началом стал гидразид изоникотиновой кислоты — производное гидразина. Другие его производные используют как средство против нервных депрессий.
А гидразид малеиновой кислоты — стимулятор роста картофеля, сахарной свеклы, винограда, табака.
Конечно, далеко не все производные гидразина применимы для подобных целей. Давно известно, что и сам гидразин, и его простейшие производные, применяемые в ракетной технике, токсичны. Сообщения о токсичности многих производных гидразина, появившиеся в медицинской литературе в последние годы, заставляют относиться к этим веществам с еще большей настороженностью и вниманием. Однако от их вредностей научились защищаться достаточно надежно.
 |
|
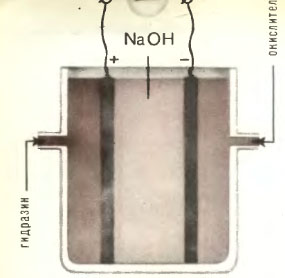
Схема гидразин-воздушиого (или гидразин-кислородного) топливного элемента |
Разработаны и кое-где уже используются на практике высокоэффективные и надежные гидразин-воздушные и гидразин-кислородные топливные элементы — химические источники тока. Они работали, в частности, вместо аккумуляторов на борту канадской одноместной научно-исследовательской подводной лодки «Стар».
При работе в топливном элементе из сравнительно ядовитого гидразина (или гидразингидрата) образуются лишь совершенно безвредные вода и азот. Электрическая энергия вырабатывается благодаря протекающей на аноде реакции:
![]()
Экологическая безвредность — главное достоинство таких источников тока.
Гидразин-воздушные топливные элементы прошли успешные испытания на микромотоцикле и грузовом электромобиле, развивавшем скорость больше 70 километров в час.
Одним словом, гидразину нашлось дело и в космосе, и под водой, и на земле.
