Микроскопия будущего
С Нобелевской премией по химии в этом году много неясного. Почему премию по химии дали за микроскопию, почему именно за эту, правда ли, что существует множество аналогичных методов? На эти и другие вопросы «Химии и жизни» отвечает кандидат биологических наук А.С.Мишин (лаборатория биофотоники Института биоорганической химии РАН).
 Александр, объясните, пожалуйста, чем замечательны методы, за которые дали премию, и есть ли у них недостатки?
Александр, объясните, пожалуйста, чем замечательны методы, за которые дали премию, и есть ли у них недостатки?
Тот и другой метод стоят очень дорого. Приборы для STED мало кто умеет производить, они сложные, дорогостоящие и ко всему прочему требуют регулярного обслуживания и поверки. Насколько мне известно, у нас в России таких систем нет, во всяком случае, мы в Москве не имеем к ним доступа.
Второй вариант микроскопии, за которую дали Нобелевскую премию, PALM, тоже многого требует, но реализовать его все-таки проще — при соблюдении определенных условий для него можно использовать почти любой микроскоп. Основное и практически достаточное требование — современная камера, обладающая чувствительностью на уровне единичных фотонов, то есть позволяющая уверенно сказать, пришло ли их 99 или 100. Такие раньше использовались в спутниках — это камеры ЕМССD или «Scientific CMOS». Конечно, есть и другие требования, но так или иначе, приблизиться к реализации микроскопии одиночных молекул в нашей стране проще — в Москве есть несколько таких систем. Но все равно это штуки, а не десятки штук. Например, мы сотрудничаем с лабораторией в Нижнем Новгороде, которая была создана по мегагранту, полученному С.А.Лукьяновым и Нижегородской государственной медакадемией («Химия и жизнь» писала об этом в № 12 за 2010 год. — Примеч. ред.). Одним из основных приобретений стал как раз такой микроскоп для детекции одиночных молекул — N-STORM произ- водства «Nikon» (STORM — STochastic Optical Reconstruction Microscopy. — Примеч. ред.).
В общем, этот вариант более доступен в России, поэтому мы сфокусировались на нем. В нашей лаборатории занимаются флуоресцентной меткой.
Раньше мы занимались в основном флуоресцентными белками, а сейчас в сотрудничестве с химиками, с группой синтеза природных соединений нашего института, пытаемся делать новый класс меток, основанных на химических красителях, но тоже пригодных для мечения живых клеток — то есть соединяющих преимущества флуоресцентных белков и химических красителей. Мы изначально планировали делать их с прицелом на эту микроскопию высокого разрешения, но до совсем недавнего времени единственная возможность работать у нас была связана с поездками в Нижний Новгород.
STORM — это то же самое, что PALM, или нет?
Это сложный вопрос. По большому счету, как раз то, что сделало присуждение Нобелевской премии, — оно стерло грань между STORM, PALM и еще несколькими десятками опубликованных вариаций методов, которые делают примерно одно и то же. Все, кто начали в этой теме работать, в какой-то момент поняли, что это интересно, и стали бороться за приоритет. Было даже не смешно: ученые образовали группы, не цитирующие друг друга, но публикующие концептуально совершенно одно и то же.
Многие удивлялись, что премию дали очень быстро, совсем немного времени прошло после основных публикаций. Конечно, тут играет роль и то, что скорость научно-технического прогресса стала почти неприлично высокой. Но могли быть и чисто «политические» причины, проблемы с приоритетом, которые начали всем осложнять жизнь. На ранней стадии несколько фирм запатентовали разные версии одной и той же микроскопии, одни и те же, по сути, вещи долгое время назывались разными именами и конкурировали между собой, причем иногда это было довольно нелепо. «Nikon» выпустила микроскоп для STORM, «Zeiss» — для PALM; технически тот и другой подходит для обоих методов, но из-за причин, связанных с патентованием, производители не имели права сообщать об этом клиентам. Только год назад они между собой договорились и стала появляться официальная информация о том, что делать это можно.
Похожая ситуация была с секвенированием.
Да, такой же мощный взрыв. Кстати, пора бы дать Нобелевскую премию и за секвенирование нового поколения. Методы примерно одинаковой свежести, но секвенирование уже сделало вещи, которые раньше были невозможными, а микроскопия сверхвысокого разрешения еще не сделала. Все поняли, что эти методы перекрывают область между оптической и электронной микроскопией. В электронной микроскопии все очень хорошо видно, но никто не знает толком, что именно, потому что невозможно мечение специфических структур.
Что бы могла сделать микроскопия сверхвысокого разрешения, если говорить о чисто практической пользе? К изучению онкологических заболеваний, которые ведутся в Нижнем Новгороде, ее не удастся привлечь?
Возможно, в идеале то, чем мы хотели бы заниматься, в тех же исследованиях с Нижним Новгородом, — это увидеть отличия на уровне ультраструктуры, например между клетками здорового пациента и пациента с онкологическим заболеванием. Онкология во многом завязана на подвижность клеток, подвижность зависит от цитоскелета, а цитоскелет — классическая модель для микроскопии сверхвысокого разрешения. Но это не относится к кругу задач, которые уже решены, это вопрос, ответ на который мы только хотели бы получить.
А какие задачи уже решены?
Например, одной из первых демонстраций возможностей метода было наблюдение прохождения единичных молекул сквозь пору в оболочке ядра клетки. Но тут выгода не только в сверхразрешении. В чем преимущество STED, несмотря на его огромную стоимость? Он уже сейчас работает, что называется, сразу после включения, для множества окрасок, для различных экспериментальных моделей, которые уже есть у исследователей, — для него не надо ничего переделывать. Он позволяет сразу ответить на вопросы вроде «нам кажется, что эти два белка взаимодействуют, так ли это?». Мы увидели на флуоресцентной микроскопии, что белки находятся рядом, однако на достаточно ли близком расстоянии, чтобы взаимодействовать? Существуют специальные методы, чтобы это установить (например, резонансный перенос энергии — FRET, см. статью Е.О.Пучкова в «Химии и жизни», 2014, № 9. — Примеч. ред.), но они не всегда удобны. А STED может быстро дать ответ на этот вопрос, по крайней мере, отрицательный. Если мы повышаем разрешение с 250 до 50 нм и видим, что белки, которые казались нам соседями, на самом деле стоят по отдельности, значит, взаимодействия нет. Кроме того, STED в той или иной степени произведен из конфокальной микроскопии, и это позволяет получать картинку препарата без режима сверхразрешения, а потом включать этот режим. Это позволяет заранее прикинуть, для какого участка нужна картинка со сверхразрешением.
А PALM такого не позволяет?
Микроскопия сверхвысокого разрешения с локализацией единичных молекул основана на разделении во времени свечения индивидуальных молекул, они должны светиться не все одновременно, а по очереди, мигая. Кстати, почему это все-таки премия за химию — микроскопия одиночных молекул первоначально была основана на мигании химических красок. Бетциг работал с флуоресцентными белками, однако на ранней стадии существования этой техники лучше всего методика получалась с химическими красками. Как выяснилось, они обладают подходящими характеристиками для такого мечения. Важно, например, чтобы молекула за время съемки камеры — 10 мс — испустила как можно больше фотонов, а на следующих кадрах, по возможности, не светилась. Если это требование выполняется, то теоретический предел достигаемого разрешения приближается к размеру молекулы, в отличие от STED, где разрешение заметно хуже. PALM/STORM при достаточной яркости источника позволяет достичь разрешения 5 нм и ниже — чем больше собираем фотонов за один кадр, тем точнее мы можем поставить центр, положение молекулы. Но таких достаточно ярких красок мало. Единичные молекулы флуоресцентных белков существенно тусклее. Есть пять-шесть белков, пригодных для микроскопии сверхвысокого разрешения, — это фотоактивируемые белки, некоторые из них не светятся вообще до того, как вы их активировали. Вот почему метод полуслепой: вы не можете сразу увидеть свою картинку обычного разрешения, а потом нужный участок в ней рассмотреть с большим разрешением — как правило, необходимо заранее знать, куда смотреть.
|
|
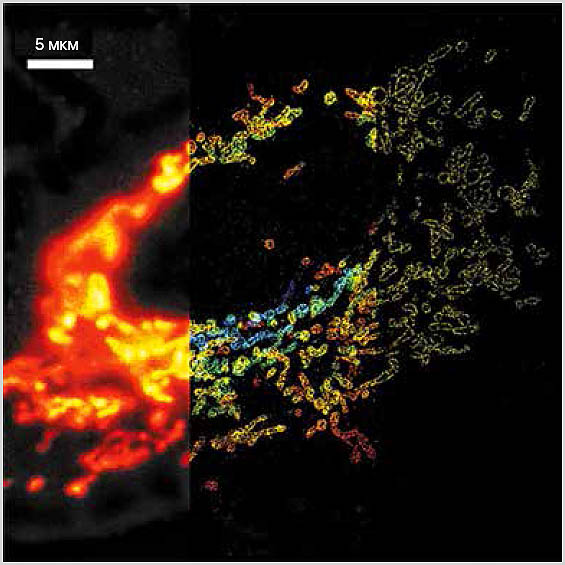
Технология 3D-STORM: митохондриальная сеть в клетке млекопитающего. Слева обычная флуоресцентная микроскопия, в центре реконструированное трехмерное изображение, справа — «срез внутри среза», изображение с тонкой плоскости. (с) Xiaowei Zhuang |
В итоге PALM/STORM позволяет получить большее разрешение, зато STED проще с точки зрения эксперимента. Видимо, со временем PALM/STORM будет удобнее, когда станут лучше флуоресцентные метки. Те флуорофоры, что существуют сейчас, — флуоресцентные белки и другие и другие популярные инструменты, — были разработаны с использованием обычных микроскопов. Армия ученых, которая их создавала и улучшала, ориентировалась на параметры, никак не связанные с микроскопией сверхвысокого разрешения. Раньше никому не было нужно, чтобы белок ярко светился в течение миллисекунд, а потом гас. Теперь, имея доступ к такого рода микроскопам, мы, в том числе и в нашей лаборатории, можем начать отбирать флуоресцентные белки, создавать более подходящие.
Как это направление будет развиваться дальше, после Нобелевской премии?
Я надеюсь, что гонка прекратится и развитие направления пойдет путем слияния методик. Что касается STED, там всегда все было очень просто. Идея на редкость изящная, она исследована и реализована технически образованными людьми и основана, строго говоря, на физическом принципе. А в микроскопии одиночных молекул, несмотря на ее колоссальный потенциал, до сих пор царит хаос. Великое множество вариантов методов приготовления препаратов, условий облучения, методов обработки изображений — тропический лес позавидовал бы такому разнообразию. Теперь, после Нобелевской премии, возможно, на- ступит более упорядоченный этап.
Строго говоря, то и другое — не первые методы наноскопии, доступные исследователям. Давно существует так называемая наноскопия ближнего поля — метод наблюдения молекул на расстояниях меньше длины волны света. Однако ограничения этого метода делают его неподходящим для биологов — например, глубина проникновения меньше, чем у любого биологического микроскопа.
А что с обработкой изображения? Тут есть перспективы?
В микроскопии одиночных молекул существует огромный потенциал для математиков. Уже появились способы реконструкции изображения сверхвысокого разрешения на основе детекции небольших флуктуаций в картинке, снятой хорошей камерой вроде тех, о которых я говорил в начале. Такая камера может безошибочно обнаружить эти флуктуации, а их анализ позволяет с помощью сложных математических методов восстановить истинное положение флуорофоров. В результате картинка с невысоким исходным разрешением, но снятая на суперчувствительную камеру реконструируется в изображение сверхвысокого разрешения. Пока что это требует очень больших вычислительных мощностей, однако сейчас это одно из самых важных направлений, как мне кажется.
Но оно интеллектоемкое.
Да.
Расскажите еще что-нибудь интересное для химиков. они опять огорчаются, что премию «отобрали» биологи…
Как я уже говорил, на ранней стадии развития метода было трудно работать с фотоактивируемыми белками: яркость у них низкая, к тому же в условиях микроскопии они быстро «сжигаются». Поэтому некоторое время чувствовалось опережение в микроскопии, основанной на химии. К этому периоду относится смешная история. Одна из задач, к которой сразу начали применять микроскопию сверхвысокого разрешения, — построение высокоточных карт мозга. Отростки, которые образуют связи между нейронами мозга, настолько тонкие, что их трудно отследить даже в срезах, — их размер сопоставим с дифракционным барьером. С другой стороны, существует такой метод построения связей между нейронами — brainbow, от brain и rainbow. Различные флуоресцентные белки случайным образом экспрессируются в мозге экспериментального животного, при этом разные нейроны помечаются разными комбинациями белков, имеют разный цвет, и это используют, чтобы отслеживать пути нервных окончаний. Исследовательница из Барселоны Мелике Лакадамияли (Melike Lakadamyali; ныне руководитель группы в барселонском Институте фотонных наук. — Примеч. ред.) применяла похожую модель, но хотела получить еще большее разрешение, чтобы разобраться в сплетении тонких отростков нейронов. Юмор заключался в том, что она красила срезы антителами к флуоресцентным белкам, а к антителам были присоединены химические краски, потому что у этих красок был существенно лучше фотонный бюджет: число фотонов, которое может испустить молекула, и это дает лучшее разрешение. Но у Лакадамияли были фиксированные образцы. Для опытов с живыми клетками и тканями, конечно, понадобятся флуоресцентные белки или иные сопоставимые по удобству метки.
У исследователей мозга есть и другие подобные проекты. Например, множество срезов смотрят сначала с помощью флуоресцентной микроскопии, а потом отправляют на электронный микроскоп, чтобы сопоставить изображения и построить корреляцию между результатами. Проекты очень трудоемкие, и всем стало бы удобнее, если бы этого не нужно было делать. Поэтому нет сомнений в том, что методы сверхвысокого разрешения быстро найдут широкое применение.
Для химиков, конечно, тоже есть много возможностей. Например, некоторые краски обратимо присоединяют меркаптоэтанол, что вызывает временный переход в темновую фазу. Есть краска, мигающая в результате спонтанном внутримолекулярной циклизации, как раз в нужной шкале времени. Сейчас, когда требуются новые краски, адаптированные к методам, вероятно, найдут свою нишу и химики, и те, кто занимаются флуоресцентными белками.
А развитие этих методов ускорит темпы исследований?
Конечно. Точно так же, как конфокальный микроскоп, в котором просто отбрасывается флуоресценция, находящаяся далеко от фокуса, — он столько дал биологии, что это трудно переоценить. Это была ситуация, очень похожая на теперешнюю: до этого на обычном микроскопе ничего не было видно в образце хоть сколько-нибудь толстом, а на конфокальном микроскопе с такими образцами стало возможно работать, и произошел колоссальный скачок. Чего-то подобного ожидают от сверхразрешающей флуоресцентной микроскопии, тем более что улучшение разрешения и отброс фона в этом случае гораздо больше, чем разница между конфокальным и обычным микроскопом.
То есть будущее покажет, в чем польза для человечества?
Да, по большому счету эта премия, мне кажется, дана авансом. Но важно то, что она разрубает гордиев узел, прекращая споры на тему «чей вклад больше».
